Por mais de um século, a desregulação energética cíclica foi reconhecida como um déficit central no transtorno afetivo bipolar (TAB) e foi descrita já em 1854 por Jean Pierre Falret em seu artigo seminal “la folie circulaire”. Emil Kraepelin observou em 1921 que durante a depressão bipolar “a ausência total de energia é especialmente evidente”. Ele também observou que durante a mania os pacientes exibem uma “energia colossal para o trabalho”, com atividade que prejudica as noites de sono.
Desde então, mais de um século de pesquisas científicas fundamentaram essas primeiras observações clínicas. Mudanças significativas no ritmo circadiano, repouso, movimento e atividade psicomotora indicam uma desregulação da geração e gasto de energia em pacientes diagnosticados com TAB. Fabricamos energia nas mitocôndrias e dados metabolômicos e de imagem indicam um papel significativo da disfunção mitocondrial no transtorno bipolar, representando alterações na produção de energia no nível celular.
Relatos de experiências vividas por pacientes com TAB relatam consistentemente mudanças no nível de energia como uma característica central da doença. Quando questionados sobre a primeira indicação perceptível de início de mania, os pacientes relataram “mudança no nível de energia” mais do que qualquer outro sintoma. Por isso, muitas pessoas com transtorno bipolar em estados maníacos, hipomaníacos e mistos praticam muito mais atividade física do que pessoas que estão deprimidas. A compulsão pelo exercício pode gerar exaustão e falta de energia, uma característica da depressão bipolar.
Comprometimento do metabolismo energético cerebral
O metabolismo da glicose e seus mecanismos reguladores desempenham um papel central na produção de energia (ATP) no corpo e no cérebro, fornecendo combustível para a fosforilação oxidativa nas mitocôndrias. A disfunção metabólica caracterizada por metabolismo anormal da glicose, disfunção mitocondrial e resistência à insulina (RI) são cada vez mais reconhecidas como características importantes na fisiopatologia do transtorno bipolar.
A geração de ATP nas mitocôndrias depende em grande parte da fosforilação oxidativa impulsionada pelo metabolismo da glicose. Evidências de espectroscopia de ressonância magnética [MRS], tomografia por emissão de pósitrons [PET] e metabolômica do sangue indicam que o metabolismo da glicose está prejudicado ou desregulado no transtorno bipolar.
O metabolismo cerebral da glicose envolve vários processos inter-relacionados pelos quais o cérebro obtém energia da glicose. Estes incluem a captação de glicose através da barreira hematoencefálica, a glicólise, que decompõe a glicose em piruvato enquanto produz energia na forma de ATP; e fosforilação oxidativa, em que o piruvato é convertido em acetil-CoA, que entra no ciclo do ácido cítrico, impulsionando a geração de ATP na cadeia de transporte de elétrons. As principais características do metabolismo desregulado da glicose observadas no transtorno bipolar são o comprometimento da fosforilação oxidativa - que é responsável pela parte mais significativa do metabolismo da glicose em condições normais - e a regulação positiva da glicólise.
A glicólise é um processo menos eficiente que a fosforilação oxidativa, produzindo apenas 2 ATP por molécula de glicose em comparação com até 36 ATP da fosforilação oxidativa. No entanto, a glicólise pode metabolizar a glicose a uma taxa muito mais rápida, permitindo ao cérebro entrar em estados de hipermetabolismo. A regulação positiva da glicólise a longo prazo em resposta à fosforilação oxidativa prejudicada representa uma adaptação patológica que ocorre em condições de disfunção mitocondrial.
Campbell, I.H., Campbell, H. The metabolic overdrive hypothesis: hyperglycolysis and glutaminolysis in bipolar mania. Mol Psychiatry 29, 1521–1527 (2024). https://doi.org/10.1038/s41380-024-02431-w
O metabolismo cerebral prejudicado da glicose também foi observado na depressão unipolar e pode, portanto, representar um marcador de déficit energético comum a vários tipos de depressão. Contudo, a desregulação do metabolismo cerebral relacionada com o humor, e não simplesmente o comprometimento crônico, parece caracterizar a perturbação bipolar. Pesquisa comparando a taxa metabólica cerebral entre estados de humor (deprimido, eutímico e maníaco) no transtorno bipolar e na depressão unipolar (deprimido e estados eutímicos) relataram um aumento significativo na taxa metabólica ao passar da depressão bipolar para o estado eutímico ou maníaco. E nenhuma mudança geral significativa na depressão unipolar ao passar do estado deprimido para o estado eutímico.
Um estudo mostrou taxas metabólicas médias do cérebro 36% mais altas na hipomania em relação aos dias de depressão. Essas características metabólicas do transtorno bipolar parecem ter uma raiz comum na disfunção dos mecanismos de sinalização da insulina, resultando em estados alternados de hipometabolismo e hipermetabolismo da glicose no cérebro.
O aumento do lactato (sangue, imagens cerebrais e líquido cefalorraquidiano) é o biomarcador mais significativamente alterado em pacientes bipolares. Indica disfunção mitocondrial. O lactato é gerado através da glicólise e, portanto, é indicativo de comprometimento da fosforilação oxidativa e aumento da produção de energia glicolítica. Outro ponto é o aumento do glutamato cerebral, uma característica central da fisiopatologia do transtorno bipolar.
Papel do glutamato no transtorno bipolar
O glutamato é um neurotransmissor excitatório. Também parece ter um papel adicional importante no transtorno bipolar, atuando como substrato energético alternativo para o ciclo do ácido tricarboxílico (TCA) através da glutaminólise, onde é convertido em alfa-cetoglutarato intermediário do ciclo de Krebs para a produção de energia.
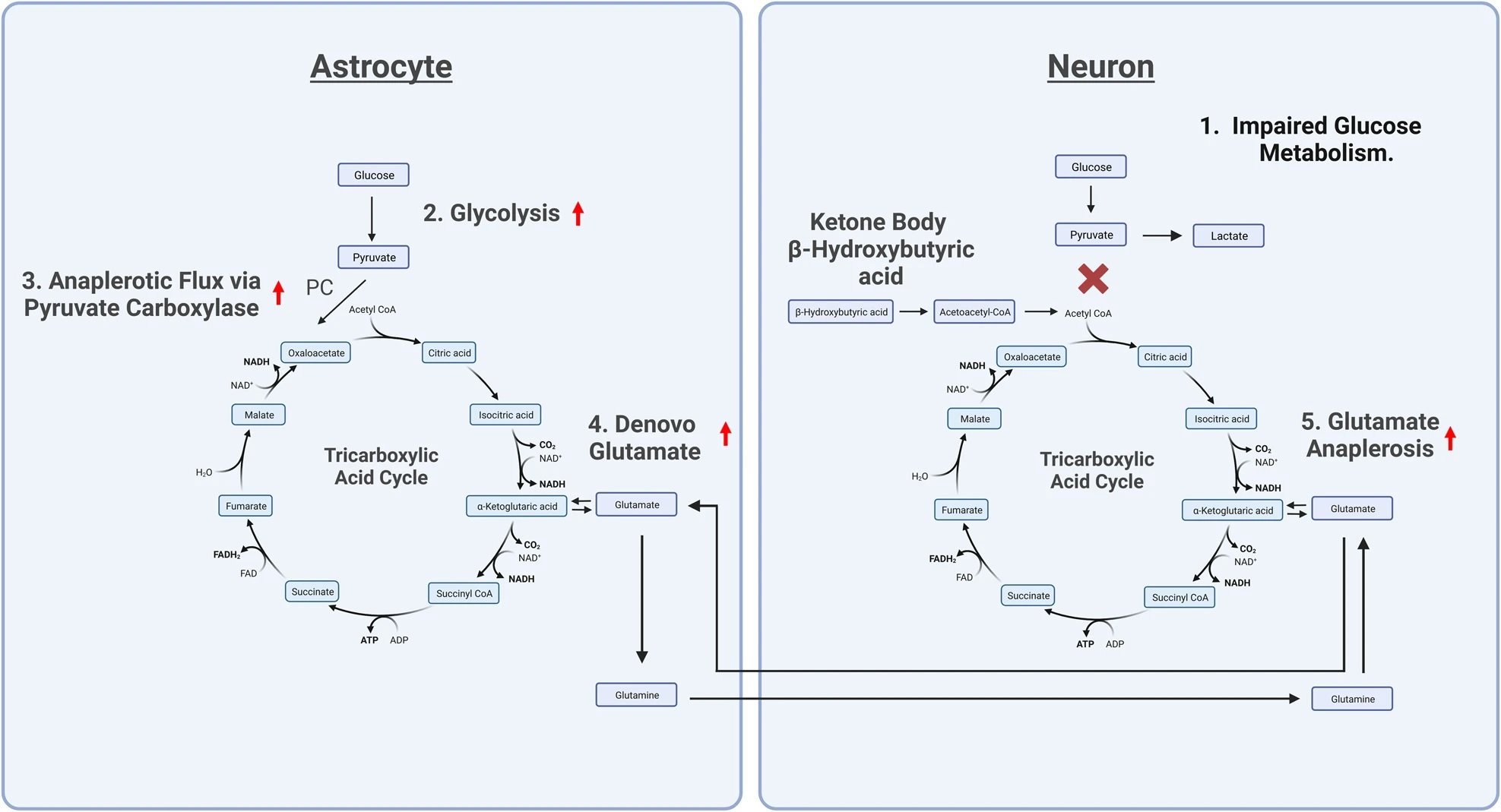
A utilização do glutamato como substrato alternativo para a produção de energia através deste mecanismo ocorre normalmente sob condições de fosforilação oxidativa prejudicada e aumento da glicólise compensatória. No cérebro, o glutamato denovo é gerado nos astrócitos e foi levantada a hipótese de que o glutamato gerado através da atividade da piruvato-carboxilase nos astrócitos pode ser responsável pelos níveis elevados de glutamato no transtorno bipolar.
Outra condição em que glutamato e lactato pode estar alterada é a epilepsia. Por isso, tanto pacientes com epilepsia, quanto pacientes com TAB são tratados com anticonvulsivantes e dieta cetogênica. A dieta ajuda a reduzir lactato e glutamato cerebral nestes pacientes, ajudando a melhorar humor e a reduzir ansiedade e impulsividade.
Os corpos cetônicos, incluindo o beta-hidroxibutirato e o acetoacetato, atuam como substratos energéticos alternativos no cérebro e demonstraram ter efeitos neuroprotetores na epilepsia e outras condições neurológicas, incluindo TAB. Mudanças significativas no metabolismo neuronal, na glicólise e no metabolismo do glutamato ocorrem no estado de cetose. Um estudo conduzido na França (imagem acima) mostrou que o a dieta cetogênica reduz sintomas depressivos dos pacientes, além de melhorar o metabolismo geral. A dificuldade maior foi a adesão à dieta restrita em carboidratos (Danan et al., 2021). Uma alternativa seria uma dieta low carb suplementada de TCM e cetonas exógenas. Conduto, poucos países possuem cetonas exógenas disponíveis. Um deles é os Estados Unidos e outro é a Inglaterra.