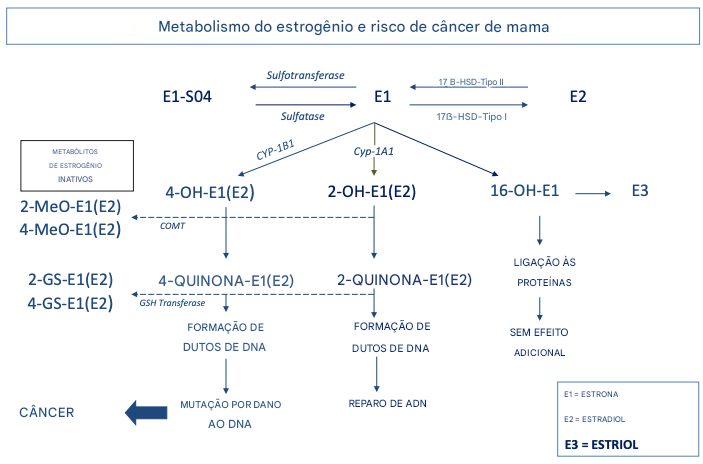
Durante muitos anos, a avaliação hormonal focou apenas na quantidade de estrogênio no organismo. Hoje sabemos que isso é insuficiente. O fator decisivo não é apenas o nível de estrogênio, mas a forma como ele é metabolizado.
O metabolismo dos estrogênios determina se essas moléculas terão um efeito mais neutro, protetor ou potencialmente perigoso para as células. Esse processo está diretamente ligado ao risco de câncer de mama, endométrio, ovário e próstata.
O que é o metabolismo dos estrogênios?
Os principais estrogênios do corpo, especialmente estradiol e estrona, passam por transformações no fígado e em outros tecidos. Esse processo gera metabólitos com comportamentos biológicos diferentes.
Existem três vias principais:
Via 2-hidroxilação (2-OH)
Via 4-hidroxilação (4-OH)
Via 16-alfa-hidroxilação (16-OH)
Cada uma dessas vias tem impacto distinto sobre proliferação celular, inflamação e dano ao DNA.
Via 2-hidroxilação: perfil mais seguro
Essa via produz metabólitos com menor atividade estrogênica e menor estímulo ao crescimento celular.
Características principais:
menor ligação ao receptor de estrogênio
menor estímulo proliferativo
eliminação mais fácil pelo organismo
menor potencial carcinogênico
Um predomínio dessa via está associado a menor risco de câncer hormônio-dependente.
Via 4-hidroxilação: maior risco genotóxico
Essa é a via mais associada ao dano direto ao DNA. Os metabólitos dessa via podem formar compostos altamente reativos que geram estresse oxidativo e mutações celulares. Esse mecanismo é considerado um dos principais elos entre estrogênio e carcinogênese.
Quando a capacidade de detoxificação é insuficiente, o risco aumenta de forma significativa.
Via 16-alfa-hidroxilação: maior estímulo proliferativo
Essa via produz metabólitos com forte atividade estrogênica. Eles permanecem ligados ao receptor por mais tempo e estimulam divisão celular. Não causam tanto dano direto ao DNA quanto a via 4-OH, mas favorecem crescimento tumoral quando presentes em excesso.
O indicador mais usado: a razão entre metabólitos
Um dos marcadores mais utilizados na prática clínica é a relação entre os metabólitos das vias 2 e 16.
Relação 2-OH / 16-OH
Interpretação prática:
relação mais alta indica perfil metabólico mais favorável
relação mais baixa indica maior estímulo proliferativo
Esse indicador não é diagnóstico de câncer. Ele é um marcador de risco biológico e de exposição hormonal ao longo do tempo.
O que realmente aumenta o risco de câncer relacionado ao estrogênio?
Os fatores mais relevantes são previsíveis e, em grande parte, modificáveis.
1) Excesso de estrogênio
Quanto maior a exposição hormonal ao longo da vida, maior o estímulo proliferativo em tecidos sensíveis ao estrogênio.
Isso pode ocorrer em situações como:
excesso de gordura corporal
resistência à insulina
terapia hormonal inadequada
menarca precoce ou menopausa tardia
baixa atividade física
2) Predominância da via 4-OH
Esse padrão aumenta a formação de metabólitos capazes de danificar o DNA.
3) Baixa capacidade de detoxificação
O organismo precisa neutralizar e eliminar metabólitos potencialmente tóxicos. Esse processo depende de enzimas envolvidas em metilação e conjugação.
As mais importantes incluem:
COMT
GST
NQO1
Quando essas vias são lentas ou sobrecarregadas, aumenta o acúmulo de metabólitos reativos.
4) Recirculação intestinal de estrogênio
O intestino tem papel direto no controle hormonal.
Quando o trânsito intestinal é lento ou existe disbiose, ocorre maior reabsorção de estrogênio, prolongando a exposição hormonal.
Situações associadas:
constipação
disbiose intestinal
inflamação intestinal
baixa ingestão de fibras
Esse mecanismo é frequentemente negligenciado, mas tem impacto clínico relevante.
Fatores que modulam o metabolismo dos estrogênios
O metabolismo hormonal responde de forma intensa ao estilo de vida e à nutrição.
Fatores que favorecem um perfil metabólico mais seguro
consumo regular de vegetais crucíferos
ingestão adequada de fibras
atividade física regular
controle da gordura corporal
função intestinal eficiente
boa capacidade de metilação
Fatores que pioram o perfil metabólico
obesidade
consumo de álcool
inflamação crônica
resistência à insulina
deficiência de nutrientes envolvidos na metilação
exposição a disruptores endócrinos
O que avaliar na prática clínica?
Uma avaliação adequada não depende de um único exame. O ideal é observar o conjunto.
Marcadores úteis:
Hormônios:
estradiol
estrona
progesterona
SHBG
Metabolismo dos estrogênios:
2-OH
4-OH
16-OH
razão 2/16
metoxiestrogênios
Capacidade de detoxificação:
homocisteína
função hepática
função intestinal
padrão alimentar
O ponto central: O estrogênio não é o problema.
O risco aparece quando existe:
exposição hormonal elevada
metabolismo desfavorável
detoxificação insuficiente
eliminação intestinal ineficiente
Esse conjunto determina o ambiente biológico onde o câncer pode ou não se desenvolver.
Em termos simples, O risco hormonal não depende apenas da quantidade de estrogênio.
Depende principalmente de três coisas:
quanto estrogênio existe
para onde ele está sendo metabolizado
se o organismo consegue eliminá-lo com eficiência
Aprenda mais sobre metabolismo nos cursos de genômica e metabolômica, com Dra. Andreia Torres.