A neurometabolômica é a aplicação da metabolômica ao sistema nervoso, com foco no estudo de metabólitos e suas alterações no cérebro e em fluidos relacionados, como o líquido cefalorraquidiano e o plasma [1] [2].
Ela auxilia na elucidação de características e alterações metabólicas em condições neurológicas, contribuindo para a descoberta de biomarcadores, a compreensão dos mecanismos das doenças e, potencialmente, para a melhoria do diagnóstico e tratamento de doenças neurodegenerativas e infecções [1] [3] [4].
Técnicas avançadas, particularmente abordagens baseadas em espectrometria de massas, permitem a caracterização de metabólitos em nível de célula única, oferecendo insights sobre diversos tipos celulares e suas alterações em estados saudáveis e patológicos [2] [5].
Entendendo a Neurometabolômica
A neurometabolômica envolve o estudo abrangente de metabólitos, que são intermediários de baixo peso molecular, no sistema nervoso central (SNC) e em biofluidos associados [1]. Este campo visa compreender como o metaboloma varia com estados fisiológicos, de desenvolvimento ou patológicos, oferecendo insights sobre o envelhecimento e doenças neurodegenerativas como a doença de Alzheimer, a doença de Parkinson e a esclerose lateral amiotrófica [1] [6] [7].
É particularmente útil para o estudo de fisiopatologias complexas, identificando impressões digitais metabólicas específicas da doença e compreendendo os mecanismos de lesão cerebral [6] [3]. A metabolômica, em geral, fornece uma leitura das atividades bioquímicas influenciadas por fatores como doenças, ambiente, medicamentos, dieta e genética, tornando-a valiosa para o diagnóstico, prognóstico e monitoramento da eficácia do tratamento [8] [9].
Aplicações e Metodologias
Avanços tecnológicos recentes, particularmente em abordagens baseadas em espectrometria de massa, têm contribuído significativamente para o avanço da metabolômica de célula única, permitindo a caracterização de moléculas importantes dentro de células individuais [2] [5]. Isso é crucial no cérebro, onde vários tipos de células estão co-localizados e apenas um subconjunto pode sofrer alterações em doenças [2]. Esses estudos podem diferenciar entre populações celulares semelhantes (por exemplo, oligodendrócitos) e diferentes tipos celulares (por exemplo, neurônios e astrócitos) e são úteis para medir alterações decorrentes de comportamento, dieta, medicamentos, atividade neuronal e doenças [2].
A neurometabolômica, especialmente quando combinada com a neurolipidômica, tem se mostrado promissora na compreensão de doenças neuroinfecciosas, identificando metabólitos e componentes lipídicos alterados no líquido cefalorraquidiano (LCR) [4]. Por exemplo, componentes lipídicos (fosfolipídios) e metabólitos como carnitina e triptofano são indicadores significativos em infecções bacterianas e virais do SNC [4]. O Consórcio de Metabolômica da Doença de Alzheimer (ADMC), em parceria com o ADNI, também está criando um banco de dados bioquímico abrangente para a doença de Alzheimer, utilizando plataformas de metabolômica e lipidômica direcionadas e não direcionadas para mapear falhas nas vias metabólicas [10].
METABOLÔMICA E DECLÍNIO COGNITIVO
Você ainda olha para o declínio cognitivo e o Alzheimer apenas como o acúmulo de proteínas beta-amiloide no cérebro? A ciência avançou, e se você é profissional de saúde, precisa acompanhar essa evolução.
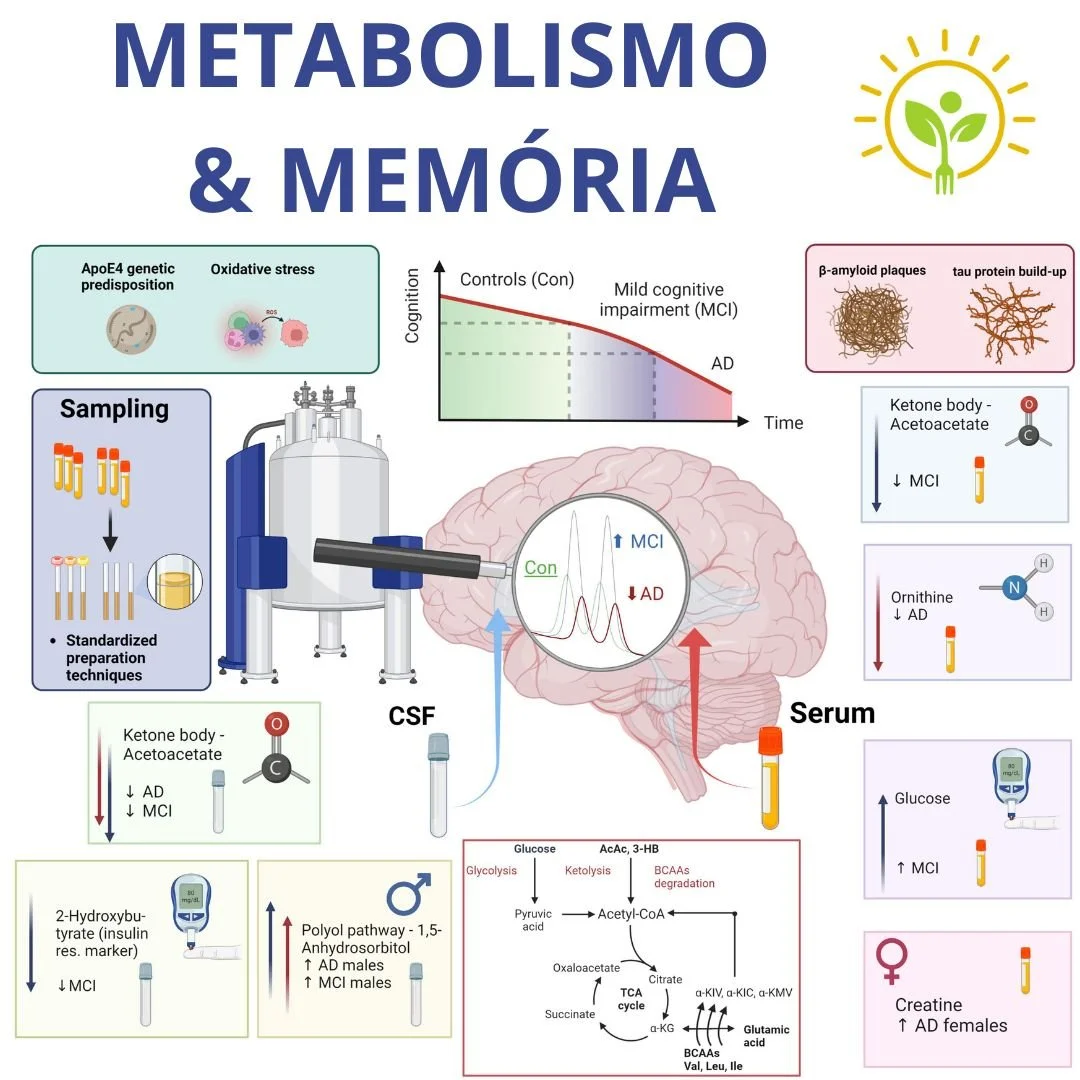
Um estudo publicado na Frontiers in Aging Neuroscience utilizou a metabolômica para mapear o que acontece no sangue e no líquor de pacientes com declínio cognitivo. O resultado? O Alzheimer é uma verdadeira crise energética e metabólica [11].
O que o exame de metabolômica revela?
1) Disfunção Energética: O cérebro em sofrimento perde a capacidade de processar glicose e tenta desesperadamente usar corpos cetônicos e aminoácidos como combustível reserva.
2) "Diabetes Tipo 3": Marcadores como o 2-hidroxibutirato mostram que a resistência à insulina está diretamente ligada à perda de memória. Por isso, tantos pacientes beneficiam-se da dieta cetogênica.
3) Assinaturas de Sexo: Homens e mulheres degradam o metabolismo de formas diferentes! Homens mostram alterações na via do poliol, enquanto mulheres apresentam picos de creatina no soro.
Como isso muda a conduta clínica❓
Se você solicita apenas exames laboratoriais básicos, está perdendo a janela de oportunidade para intervir no Comprometimento Cognitivo Leve (CCL) e prevenir o Alzheimer. A metabolômica e a genética permitem que você enxergue o incêndio antes que a casa seja destruída.
Não basta diagnosticar a doença; é preciso entender a rota metabólica que levou o paciente até ali. Qual suplementação ele realmente precisa? Qual dieta vai poupar sua reserva cognitiva baseada no seu polimorfismo genético?
🚀 DOMINE A CIÊNCIA DE PRECISÃO
A interpretação desses dados é o que diferencia o profissional generalista do especialista de elite. Se você quer aprender a ler essas "assinaturas biológicas" e transformar a vida dos seus pacientes com tratamentos personalizados.
Conheça o Curso de Interpretação de Exames Genéticos e Metabolômicos.
Aprenda a transformar dados complexos em condutas práticas e eficazes. O futuro da saúde não é clínico, é molecular.
🔗 Toque no link da bio ou acesse: https://bit.ly/genomica-visual
Referências
1) M Jové et al. Metabolomics of human brain aging and age-related neurodegenerative diseases. Journal of neuropathology and experimental neurology (2014). https://pubmed.ncbi.nlm.nih.gov/24918636/
2) M Qi et al. Single Cell Neurometabolomics. ACS chemical neuroscience (2017). https://pubmed.ncbi.nlm.nih.gov/28982006/
3) À García-Cazorla et al. Cellular neurometabolism: a tentative to connect cell biology and metabolism in neurology. Journal of inherited metabolic disease (2018). https://pubmed.ncbi.nlm.nih.gov/30014209/
4) ON Plaatjie et al. LC-MS metabolomics and lipidomics in cerebrospinal fluid from viral and bacterial CNS infections: a review. Frontiers in neurology (2024). https://pubmed.ncbi.nlm.nih.gov/39161867/
5) XW Zhang et al. Mass spectrometry-based metabolomics in health and medical science: a systematic review. RSC advances (2020). https://pubmed.ncbi.nlm.nih.gov/35497733/
6) J Troisi et al. Metabolomics in Parkinson's disease. Advances in clinical chemistry (2021). https://pubmed.ncbi.nlm.nih.gov/34462054/
7) H Blasco et al. Metabolomics in amyotrophic lateral sclerosis: how far can it take us?. European journal of neurology (2016). https://pubmed.ncbi.nlm.nih.gov/26822316/
8) J Troisi et al. Metabolomics in genetic testing. Advances in clinical chemistry (2020). https://pubmed.ncbi.nlm.nih.gov/31952575/
9) DS Wishart et al. Emerging applications of metabolomics in drug discovery and precision medicine. Nature reviews. Drug discovery (2016). https://pubmed.ncbi.nlm.nih.gov/26965202/
10) L St John-Williams et al. Targeted metabolomics and medication classification data from participants in the ADNI1 cohort. Scientific data (2017). https://pubmed.ncbi.nlm.nih.gov/29039849/
11) G Berezhnoy et al. Metabolomic profiling of CSF and blood serum elucidates general and sex-specific patterns for mild cognitive impairment and Alzheimer's disease patients. Front Aging Neurosci. 2023 Aug 24;15:1219718. doi: 10.3389/fnagi.2023.1219718. PMID: 37693649; PMCID: PMC10483152.