O artigo "Minerals and the Menstrual Cycle: Impacts on Ovulation and Endometrial Health", publicado na revista Nutrients em março de 2024, oferece uma análise abrangente sobre o papel dos minerais essenciais na saúde reprodutiva feminina, com foco na regulação hormonal, função ovariana, ovulação, saúde endometrial e estresse oxidativo ao longo do ciclo menstrual.
Visão Geral do Ciclo Menstrual e Função Reprodutiva
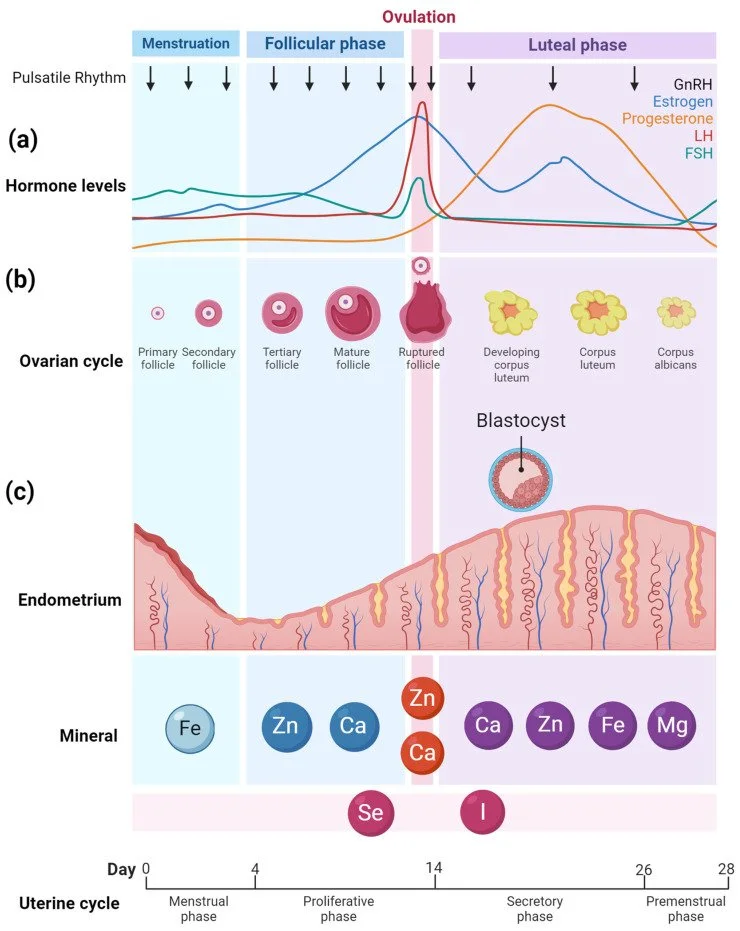
O ciclo menstrual é regulado por hormônios que guiam processos desde o início da menstruação até a ovulação e gestação. Durante a fase folicular, o hormônio folículo-estimulante (FSH) promove o crescimento dos folículos ovarianos, levando ao aumento dos níveis de estrogênio, que por sua vez suprimem a produção de FSH. Na fase luteínica, a progesterona prepara o endométrio para uma possível gravidez. Distúrbios nesses processos podem resultar em irregularidades menstruais, anovulação e dificuldades na concepção.
Minerais Essenciais e Seus Efeitos no Ciclo Menstrual
1. Zinco (Zn)
Função: Essencial para a síntese de hormônios esteroides, desenvolvimento folicular e ovulação.
Efeito: Níveis baixos de zinco podem alterar a produção de FSH e LH, levando a irregularidades menstruais.
2. Magnésio (Mg)
Função: Atua como cofator em mais de 600 reações enzimáticas, incluindo a função antioxidante.
Efeito: Níveis insuficientes podem aumentar o estresse oxidativo e prejudicar a função reprodutiva.
3. Cálcio (Ca)
Função: Contribui para a secreção do GnRH, desenvolvimento folicular e liberação do oócito durante a ovulação.
Efeito: Desequilíbrios nos níveis de cálcio podem comprometer a fertilidade e o sucesso da gravidez.
4. Iodo (I)
Função: Essencial para a função tireoidiana e equilíbrio hormonal.
Efeito: A deficiência pode levar a hipotiroidismo, afetando a ovulação e a fertilidade feminina.
5. Selênio (Se)
Função: Protege os tecidos reprodutivos contra danos oxidativos, promovendo ovulação estável e preservando a função ovariana.
Efeito: Níveis ideais de selênio estão associados a melhores resultados de fertilidade.
6. Ferro (Fe)
Função: Importante para a saúde endometrial e implantação embrionária.
Efeito: Desequilíbrios nos níveis de ferro podem afetar a fertilidade e o sucesso da gravidez.
7. Cobre (Cu)
Função: Cofator para a enzima superóxido dismutase (Cu,Zn-SOD), ajudando a proteger os oócitos contra o estresse oxidativo.
Efeito: Excessos de cobre podem induzir estresse oxidativo; portanto, o equilíbrio é crucial.
8. Manganês (Mn)
Função: Atua como cofator para a enzima manganês superóxido dismutase (Mn-SOD), protegendo as células contra o estresse oxidativo.
Efeito: Deficiências podem comprometer a qualidade dos oócitos e o equilíbrio hormonal.
Considerações Importantes
Embora a suplementação de minerais seja benéfica em casos de deficiência diagnosticada, o uso indiscriminado pode ser prejudicial. É fundamental que a suplementação seja orientada com base em sua individualidade. Quer se cuidar melhor para engravidar? Marque sua consulta de nutrição aqui.
Uma dieta equilibrada é fundamental para a manutenção da saúde reprodutiva feminina. A orientação profissional é crucial para garantir que as necessidades nutricionais sejam atendidas adequadamente, promovendo a fertilidade e o bem-estar geral.