Evidências de diversas áreas de pesquisa, incluindo cronobiologia, metabolômica e espectroscopia de ressonância magnética, indicam que a desregulação energética é uma característica central da fisiopatologia do transtorno bipolar.
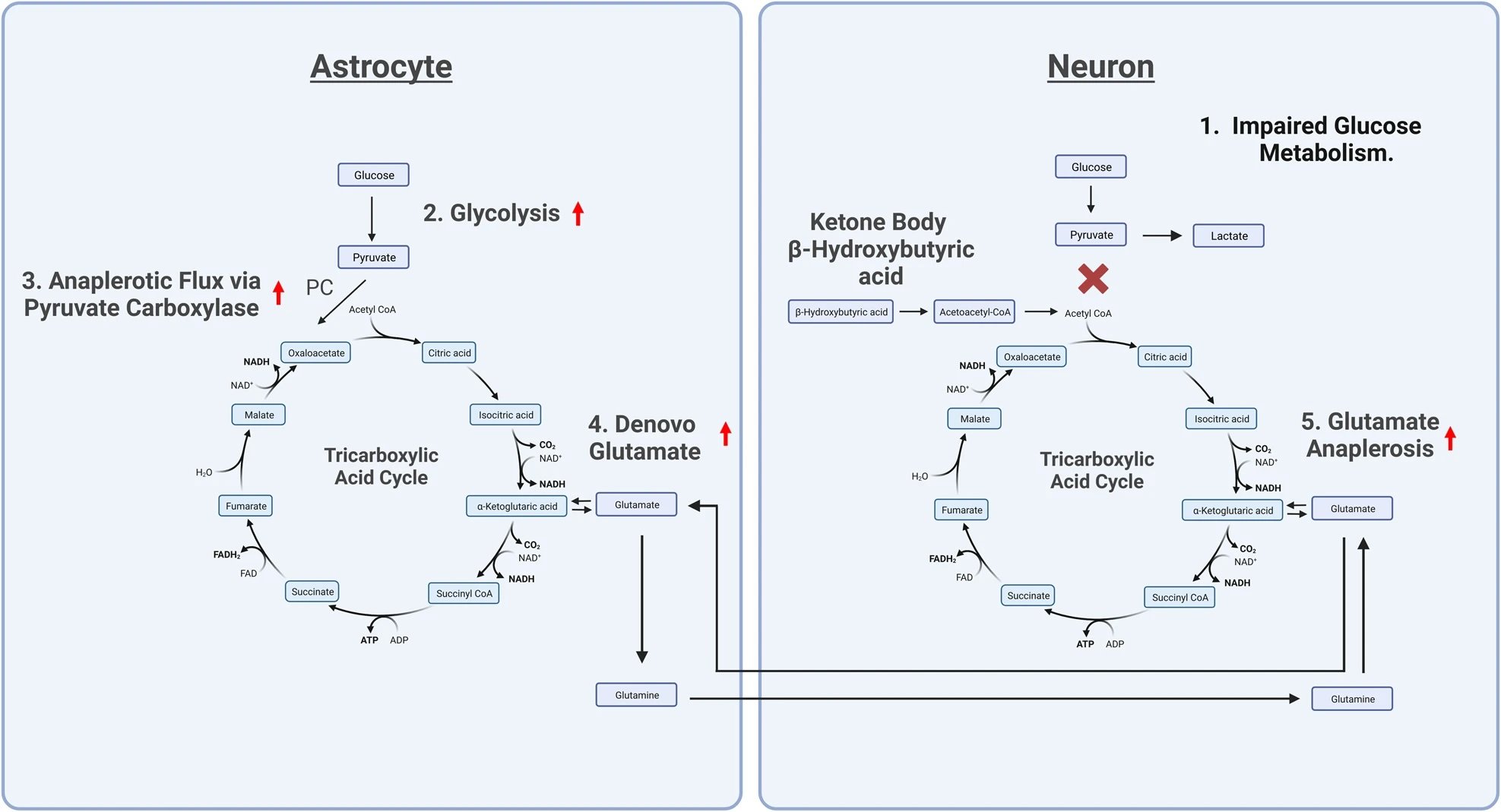
Pesquisas mostram que a mania pode representar uma condição de metabolismo energético cerebral aumentado, facilitado pela hiperglicólise e glutaminólise. Quando o metabolismo oxidativo da glicose fica prejudicado no cérebro, os neurônios podem utilizar o glutamato como substrato alternativo para gerar energia através da fosforilação oxidativa.
A glicólise nos astrócitos alimenta a formação de glutamato denovo, que pode ser usado como fonte de combustível mitocondrial em neurônios via transaminação para alfa-cetoglutarato e subsequente carboxilação redutiva para reabastecer os intermediários do ciclo do ácido tricarboxílico. A regulação positiva da glicólise e da glutaminólise dessa maneira faz com que o cérebro entre em um estado de metabolismo intensificado e atividade excitatória que pode estar por trás dos episódios de mania.
Campbell, & Campbell, 2024. https://doi.org/10.1038/s41380-024-02431-w
Em condições normais, este mecanismo desempenha uma função adaptativa para regular positivamente o metabolismo cerebral em resposta à demanda aguda de energia. No entanto, quando recrutado a longo prazo para neutralizar o metabolismo oxidativo prejudicado, pode tornar-se um processo patológico.
A causa exata do metabolismo desregulado da glicose no bipolar não é conhecida, no entanto, a disfunção endocrinológica, como a hiperinsulinemia, pode aplicar uma carga alostática que inicia e/ou acelera o curso da doença naqueles que são geneticamente suscetíveis. Por exemplo, pessoas com diabetes tipo 2 ou resistência à insulina têm probabilidades três vezes maiores de desenvolver uma doença crónica em comparação com aquelas com glicemia normal.
O que é carga alostática?
A carga alostática é um conceito fundamental para entender os impactos do estresse crônico na saúde. Imagine seu corpo como um carro: quando você acelera e freia constantemente, desgasta as peças mais rápido. A carga alostática é esse desgaste causado pela ativação frequente dos sistemas do corpo em resposta a estressores.
Em termos mais técnicos, a carga alostática representa a ativação repetida e prolongada dos sistemas neuroendócrino, imunológico, metabólico e cardiovascular. Essa ativação constante gera um desequilíbrio homeostático, ou seja, o corpo não consegue mais manter seu estado de equilíbrio interno.
Como a Carga Alostática Afeta a Saúde?
Uma alta carga alostática está associada a um risco aumentado de diversas doenças, como:
Doenças cardiovasculares: Hipertensão, infarto, derrame.
Doenças metabólicas: Diabetes, obesidade.
Doenças mentais: Depressão, ansiedade, TAB.
Doenças autoimunes: Lúpus, artrite reumatoide.
Doenças neurodegenerativas: Alzheimer, Parkinson.
Fatores que Contribuem para a Carga Alostática
Genética: Variações genéticas podem afetar a sensibilidade e a reatividade dos sistemas de resposta ao estresse do corpo, como o eixo hipotálamo-hipófise-adrenal (HPA). Indivíduos com certas variantes genéticas podem ser mais propensos ao estresse crônico e à carga alostática elevada. Fatores genéticos também podem influenciar os processos metabólicos, afetando como o corpo regula a glicose, a insulina e outros hormônios. Enfim, a genética pode impactar o funcionamento do sistema imunológico, afetando sua capacidade de responder a estressores e manter o equilíbrio. A desregulação do sistema imunológico pode levar à inflamação crônica e ao aumento da carga alostática.
Estresse crônico: Trabalho excessivo, problemas financeiros, relacionamentos conflituosos.
Traumas: Abusos, perdas, catástrofes.
Inflamação crônica: Causada por doenças ou hábitos de vida não saudáveis.
Desordens do sono: Insônia, apneia do sono.
Fatores sociais: Discriminação, desigualdade social.
Como Reduzir a Carga Alostática?
Embora a carga alostática seja um processo complexo, existem estratégias para reduzir seus efeitos:
Gerenciamento do estresse: Pratique técnicas de relaxamento como meditação, yoga, respiração profunda.
Sono de qualidade: Durma pelo menos 7-8 horas por noite.
Exercício físico regular: Pratique atividades que você gosta.
Fortalecimento das relações sociais: Conecte-se com amigos e familiares.
Terapia: Procure ajuda profissional para lidar com traumas e emoções difíceis.
Alimentação saudável: Evitar alimentos ultraprocessados, corantes, conservantes, alérgenos é fundamental. Ter uma dieta e suplementação que forneçam os nutrientes adequados também. Estudos também mostram que a dieta cetogênica seria uma alternativa para a correção da desregulação energética cerebral.
Os corpos cetônicos podem ser utilizados como uma fonte alternativa de combustível neuronal à glicose, que contorna a glicólise. Agem de maneira semelhante ao glutamato, fornecendo um substrato energético alternativo para a fosforilação oxidativa. No entanto, os corpos cetônicos não dependem da regulação positiva da glicólise e, em contraste com as propriedades excitatórias do glutamato, podem promover níveis mais elevados do neurotransmissor inibitório GABA, relaxando o cérebro.
Essas características distintas dos corpos cetônicos permitem restaurar a fosforilação oxidativa quando o metabolismo da glicose está prejudicado, sem a necessidade de induzir hiperglicólise ou altos níveis de glutamato e atividade excitotóxica no cérebro. A cetose também ajuda a reduzir os níveis de glutamato no cérebro. O beta-hidroxibutirato reduz os níveis de glutamato e atua como um inibidor de glutamato nos receptores NMDA. As cetonas podem, portanto, atuar na prevenção de episódios maníacos, eliminando a necessidade de utilização do glutamato como substrato energético alternativo quando o metabolismo oxidativo normal da glicose está prejudicado.
Aprenda mais em https://t21.video