A barreira hematoencefálica é composta por várias membranas que separam o sistema nervoso central (SNC) do sistema circulatório periférico. O objetivo dessa barreira é permitir a passagem de nutrientes e sinais celulares da corrente sanguínea para os nervos e células de suporte no SNC, excluindo substâncias nocivas.
Predisposições genéticas, exposições ambientais e envelhecimento podem enfraquecer a integridade dessa barreira, permitindo que endotoxinas e células imunes inflamatórias se infiltrem no cérebro, contribuindo para o envelhecimento acelerado do cérebro e para o aumento do risco de doenças neurodegenerativas, como a doença de Alzheimer, doença de Parkinson e esclerose múltipla.
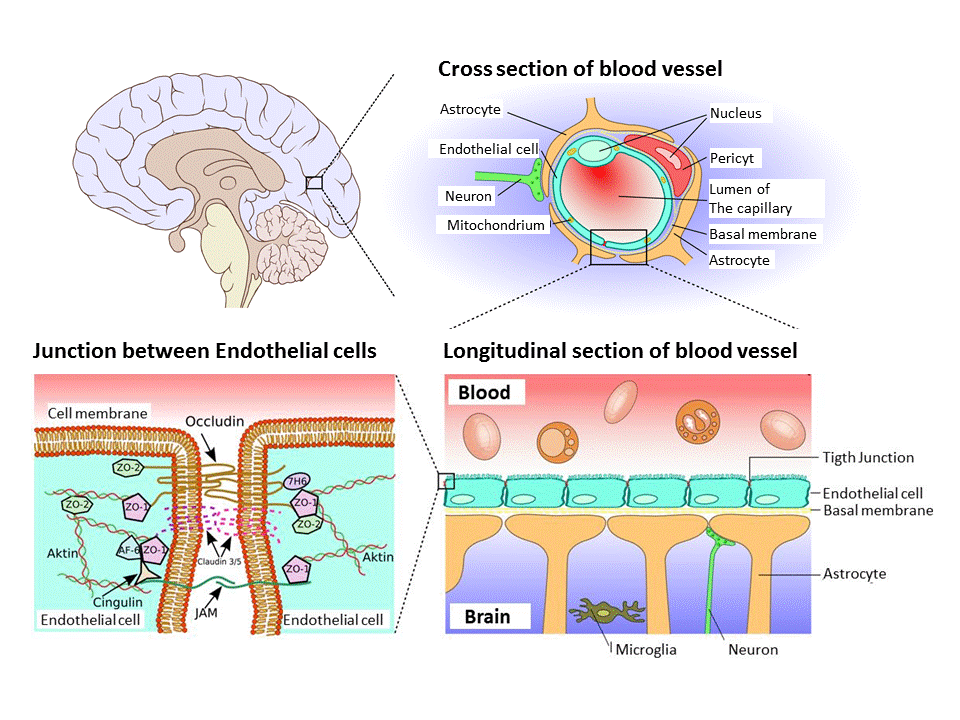
Anatomia da barreira hematoencefálica
Os vasos sanguíneos em todo o corpo são revestidos por uma única camada de células endoteliais, um tipo especializado de célula epitelial. O lado luminal (interno) da folha endotelial faz interface diretamente com a corrente sanguínea e contém transportadores que trocam nutrientes e resíduos.
FSM (basic artwork: wikimedia commons)
O lado basal (externo) do endotélio na barreira hematoencefálica se conecta principalmente aos pericitos, que são células polivalentes que controlam a dilatação e a constrição dos vasos sanguíneos e secretam sinais parácrinos e endócrinos. Astróglia, células em forma de estrela com muitos braços, conectam o endotélio e os pericitos do sistema vascular aos neurônios no SNC.
Essa estrutura multicelular e seus muitos conjuntos de membranas de conexão são chamados de unidade neurovascular e servem ao propósito de troca de nutrientes e resíduos, ao mesmo tempo em que fornecem muitos pontos de regulação para evitar danos neuronais. Além de criar conexões entre os vasos sanguíneos e os neurônios, os astrócitos também conectam os vasos sanguíneos entre si, formando um circuito para eliminação de resíduos, chamado de sistema glinfático.
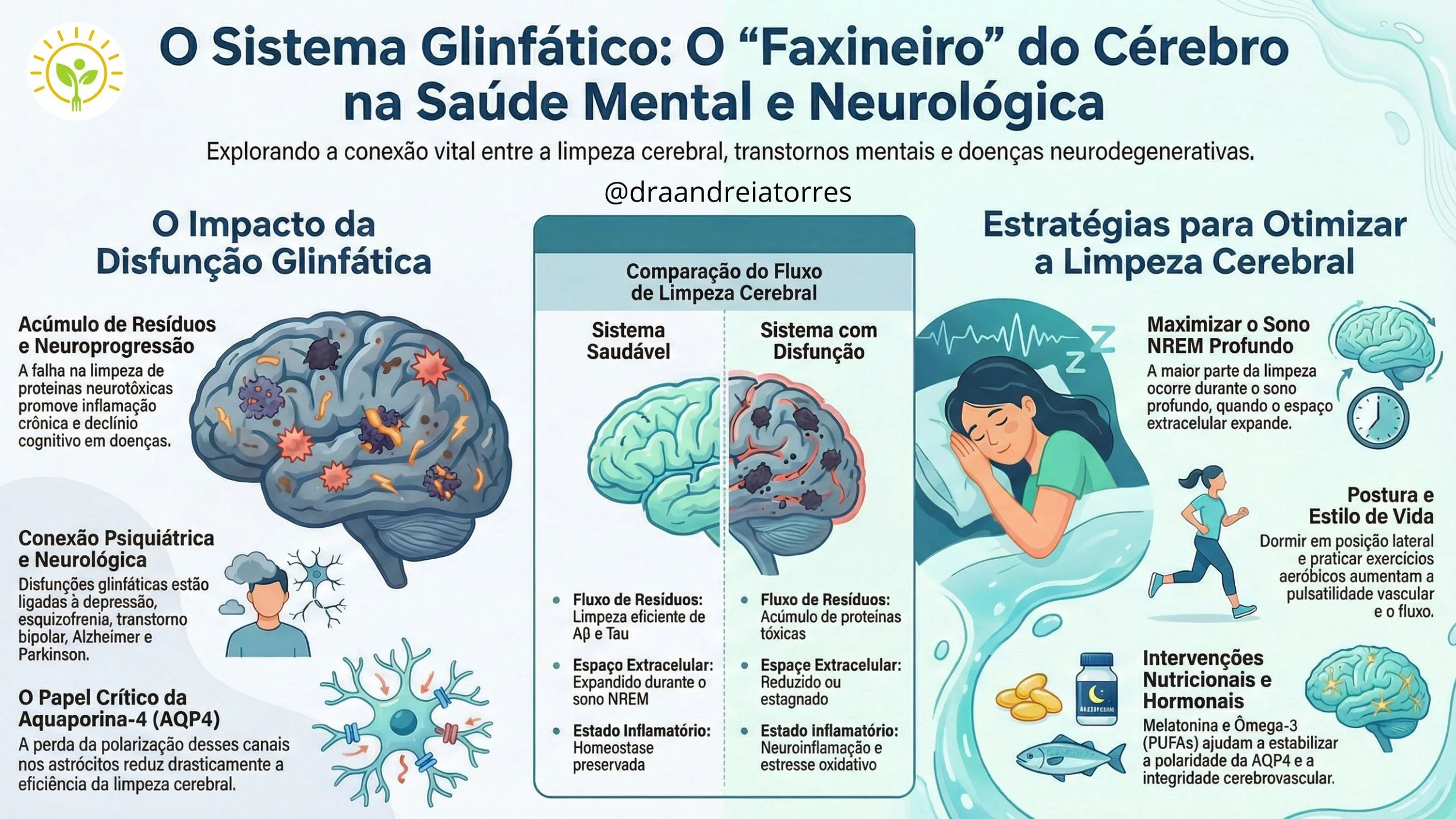
Este sistema de movimento de fluido altamente controlado é responsável pela eliminação de resíduos durante o sono, lesões e doenças porque, ao contrário de outros órgãos, o cérebro não possui estruturas linfáticas tradicionais. A disfunção glinfática perturba a pressão normal no cérebro e prejudica a eliminação de resíduos, contribuindo para a neurodegeneração e transtornos psiquiátricos (Wang et al., 2025).
Fatores ambientais importantes para melhoria da função da barreira hematoencefálica
Ácidos graxos ômega-3 - Os ômega-3, particularmente o DHA de origem marinha, regulam o transporte através da barreira hematoencefálica. Gorduras insaturadas constroem membranas flexíveis e eficientes. O DHA, em especial, bloqueia a entrada de toxinas e infecções suprimindo a transcitose na barreira hematoencefálica.
Polifenóis - Polifenóis e outros fitonutrientes de alimentos à base de plantas aumentam os metabólitos neuroprotetores na barreira hematoencefálica.
Obesidade - A obesidade aumenta a endotoxemia e a ativação do receptor toll-likedevido à permeabilidade intestinal perturbada e hiperglicemia, interrompendo a função da barreira hematoencefálica.
Exercício aeróbico - O exercício reduz as alterações relacionadas à idade na barreira hematoencefálica que aumentam o vazamento e a neurodegeneração.
Interdependência entre as barreiras intestinal e cerebral
A barreira intestinal é a maior interface de membrana entre o corpo e o mundo exterior. Semelhante a todas as barreiras membranosas, serve ao propósito de trocar nutrientes e resíduos, mas em uma escala exponencialmente maior do que a maioria. Também semelhante a outras barreiras membranosas, a barreira intestinal perde função com a idade e a doença. O aumento da permeabilidade intestinal, também conhecido como "intestino permeável", compromete a saúde de todo o corpo ao permitir a passagem de patógenos e toxinas de alimentos e bebidas para a corrente sanguínea.
Ao contrário da barreira hematoencefálica, a barreira intestinal tem a complexidade adicional de interagir com a microbiota intestinal, a comunidade de microorganismos que habita o trato digestivo. A fim de manter a distância entre as células intestinais e os patógenos e toxinas que se deslocam pelo trato digestivo, a barreira intestinal utiliza estratégias físicas, químicas e biológicas.
O epitélio intestinal contém células caliciformes que secretam uma camada de muco protetor que restringe o crescimento de bactérias e o movimento de toxinas. As células imunes localizadas no epitélio intestinal secretam fatores imunológicos na camada de muco, permitindo que bactérias amigáveis colonizem o espaço próximo à barreira, expulsando micróbios desconhecidos. Quandoesse complexo sistema de filtragem enfraquece, os níveis de toxinas microbianas na corrente sanguínea aumentam, uma condição conhecida como endotoxemia.
A hiperpermeabilidade intestinal causa endotoxemia e acelera o envelhecimento cerebral. A endotoxina mais comum encontrada na circulação é o lipopolissacarídeo (LPS), uma estrutura lipídica e de carboidratos liberada das paredes celulares de bactérias Gram-negativas, como Escherichia coli.
Pessoas com distúrbios intestinais, como doença celíaca e doença inflamatória intestinal, apresentam ruptura crônica da barreira e endotoxemia. Esse fenômeno também ocorre em doenças como obesidade e diabetes tipo 2, que são caracterizadas por endotoxemia metabólica, uma elevação crônica de duas a três vezes nas endotoxinas que aumenta a inflamação de todo o corpo e contribui para a resistência à insulina e ganho de peso.
Muitas doenças envolvendo o cérebro também compartilham endotoxemia leve crônica como uma característica, incluindo distúrbios do neurodesenvolvimento, como transtorno do espectro autista, doenças neuropsiquiátricas, como depressão e doenças neurodegenerativas, como doença de Alzheimer e doença de Parkinson.
A pesquisa que investiga o papel do eixo intestino-cérebro na doença de Alzheimer fornece uma maior compreensão de como a endotoxemia afeta a barreira hematoencefálica e melhora a saúde do cérebro no contexto do envelhecimento. O corpo de pesquisa disponível demonstra que alterações na composição da microbiota intestinal reduzem a integridade da barreira intestinal e expõem o sistema imunológico a padrões moleculares associados a patógenos, como o LPS. O LPS é interceptado pelo receptor toll-like (TLR)4 em monócitos e células endoteliais, causando inflamação sistêmica que aumenta a permeabilidade da barreira hematoencefálica e promove a neurodegeneração.
A permeabilidade da membrana é necessária para recrutar células imunes e nutrientes para áreas danificadas durante uma infecção ou após uma lesão. Padrões moleculares associados a danos (DAMPs), como a proteína do grupo de alta mobilidade (HMG)-1, uma proteína que organiza a cromatina e controla a transcrição do DNA, também se ligam a receptores imunológicos que estimulam a inflamação. No caso da ativação do receptor DAMP, as células da barreira hematoencefálica recrutam células imunes fagocíticas (ou seja, comedoras de células), como monócitos, para limpar os detritos celulares e estimular o reparo.
Obesidade e a barreira hematoencefálica
Na obesidade, os tecidos sensíveis à insulina, como fígado, tecido adiposo e músculo esquelético, são sobrecarregados por uma ingestão crônica de calorias em excesso, geralmente de alimentos com alto índice glicêmico. Para se proteger do estresse oxidativo causado pelo excesso de ingestão calórica, essas células reduzem sua capacidade de resposta à insulina. À medida que a resistência à insulina piora, os níveis de açúcar no sangue tornam-se cronicamente elevados, levando à remodelação a longo prazo da barreira hematoencefálica. As alterações incluem espessamento das membranas, redução do fluxo sanguíneo e aumento da permeabilidade.
Os produtos finais de glicação avançada (AGEs) reduzem diretamente a expressão das proteínas de junções estreitas nos pericitos, permeabilizando a barreira hematoencefálica e aumentando a produção de citocinas pró-inflamatórias.
Uma razão para esse aumento da permeabilidade é a produção de produtos finais de glicação avançada (AGEs), que são estruturas lipídicas e proteicas que foram glicadas, ou seja, ligadas quimicamente à glicose. Os AGEs reduzem diretamente a expressão das proteínas da junção estreita nos pericitos, permeabilizando a barreira hematoencefálica e aumentando a produção de citocinas pró-inflamatórias.
A obesidade prejudica ainda mais a barreira hematoencefálica ao reduzir a expressão de proteínas do citoesqueleto necessárias para sustentar a barreira; proteínas de transporte que facilitam a troca de nutrientes e resíduos; e proteínas funcionais, como enzimas, acompanhantes e fatores de transcrição. Por sua vez, a barreira hematoencefálica é menos capaz de transportar hormônios supressores do apetite, como a leptina, para o SNC. Sem os sinais adequados de saciedade, as pessoas tendem a comer demais, promovendo mais ganho de peso.
Reversão da resistência insulínica repara barreira hematoencefálica
Estudo publicado em 2022 mostrou a importância da reversão da resistência insulínica para reparo da barreira hematoencefálica e tratamento de depressão, transtorno bipolar e declínio cognitivo.
São muitas as intervenções neuroprotetoras para tratamento da doença de Alzheimer. Precisamos reverter a neuroinflamação, proteger neurônios e astrócitos, remielinizar, regular o metabolismo da glicose, proteger o sistema vascular e linfática, eliminar substâncias neurotóxicas, aumentar exercício físico, melhorar alimentação e suplementação (Liu et al., 2024).
Aprenda mais em https://t21.video