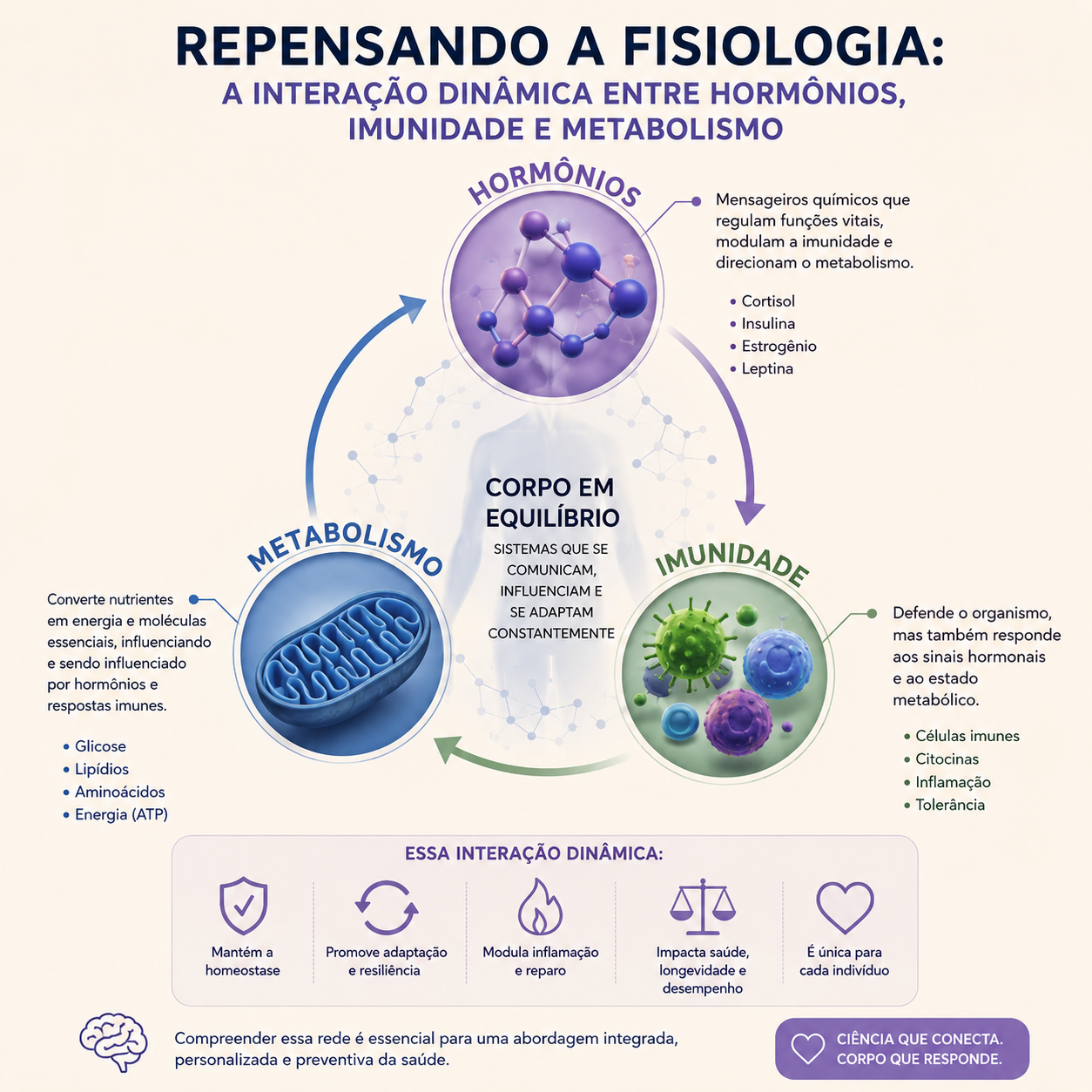
Durante décadas, a fisiologia humana foi estudada de forma fragmentada. O sistema endócrino era analisado separadamente do sistema imunológico, enquanto o metabolismo era frequentemente reduzido à produção e utilização de energia. Essa visão compartimentalizada contribuiu para avanços importantes na medicina, mas tornou-se insuficiente para explicar a complexidade das doenças crônicas modernas.
Hoje, a ciência reconhece que hormônios, sistema imune e metabolismo formam uma rede integrada, dinâmica e bidirecional. Alterações em um desses sistemas inevitavelmente repercutem nos outros. Inflamação altera a sinalização hormonal, hormônios modulam respostas imunes e o estado metabólico influencia profundamente a função celular.
Essa nova perspectiva muda não apenas a compreensão da fisiologia humana, mas também a forma como interpretamos doenças como obesidade, diabetes tipo 2, síndrome metabólica, doenças autoimunes, infertilidade, depressão, neuroinflamação e envelhecimento acelerado.
O Fim da Visão Compartimentalizada
Tradicionalmente, a endocrinologia focava em glândulas e hormônios, a imunologia em defesa contra patógenos e a bioquímica metabólica em vias energéticas. Entretanto, estudos das últimas décadas demonstraram que essas áreas são profundamente interdependentes.
O tecido adiposo, por exemplo, deixou de ser considerado apenas um reservatório energético. Hoje sabemos que ele funciona como um órgão endócrino e imunológico ativo, produzindo adipocinas inflamatórias, citocinas e sinais hormonais capazes de alterar sensibilidade à insulina, função ovariana, atividade tireoidiana e neuroinflamação.
Da mesma forma, células imunológicas respondem continuamente a sinais metabólicos. Linfócitos, macrófagos e células dendríticas alteram seu comportamento conforme disponibilidade de glicose, aminoácidos, ácidos graxos e oxigênio.
A fisiologia moderna passa a ser entendida como um sistema adaptativo integrado.
Hormônios: Muito Além da Reprodução e do Crescimento
Hormônios não atuam apenas como mensageiros isolados. Eles são reguladores centrais da inflamação, da utilização energética e da sobrevivência celular.
Cortisol
O cortisol é um exemplo clássico dessa integração. Em situações agudas, ele possui efeito anti-inflamatório importante e ajuda na adaptação ao estresse. Porém, ativação crônica do eixo hipotálamo-hipófise-adrenal altera profundamente a imunidade e o metabolismo.
Excesso persistente de cortisol está associado a:
resistência à insulina;
redistribuição de gordura visceral;
perda muscular;
disfunção mitocondrial;
aumento de permeabilidade intestinal;
supressão imune inicial seguida de inflamação crônica de baixo grau.
Além disso, o cortisol interfere diretamente na sinalização tireoidiana, gonadal e neurotransmissora.
Insulina
A insulina também deixou de ser vista apenas como hormônio glicêmico. Ela atua sobre inflamação, função endotelial, expressão gênica e plasticidade cerebral.
Resistência à insulina está relacionada a:
aumento de citocinas pró-inflamatórias;
ativação de NF-kB;
estresse oxidativo;
disfunção mitocondrial;
alterações cognitivas;
maior risco cardiovascular.
A hiperinsulinemia crônica funciona como um estado pró-inflamatório sistêmico.
Estrogênio
O estrogênio apresenta efeitos complexos sobre imunidade e metabolismo. Dependendo do contexto fisiológico, pode exercer ações anti-inflamatórias ou pró-inflamatórias.
Ele influencia:
ativação de linfócitos;
produção de anticorpos;
metabolismo mitocondrial;
sensibilidade à insulina;
função vascular;
neuroproteção.
Isso ajuda a explicar por que mulheres possuem maior prevalência de doenças autoimunes, mas também maior proteção cardiovascular antes da menopausa.
O Sistema Imune como Sensor Metabólico
O sistema imunológico não reage apenas a vírus e bactérias. Ele monitora constantemente o estado energético do organismo.
Células imunes dependem de vias metabólicas específicas para desempenhar suas funções.
Macrófagos pró-inflamatórios, por exemplo, utilizam predominantemente glicólise rápida, enquanto células reguladoras e anti-inflamatórias dependem mais da fosforilação oxidativa mitocondrial.
Isso significa que:
excesso de glicose;
lipotoxicidade;
hipoxia tecidual;
deficiência de micronutrientes;
disfunção mitocondrial;
alterações do microbioma;
podem modificar diretamente o comportamento imunológico.
A inflamação crônica de baixo grau observada na obesidade e na síndrome metabólica representa um exemplo claro dessa interação.
Imunometabolismo: Uma Nova Fronteira
O conceito de imunometabolismo surgiu para descrever como vias metabólicas regulam respostas imunes e vice-versa.
Hoje sabemos que metabólitos não são apenas produtos finais bioquímicos. Muitos atuam como moléculas sinalizadoras.
Exemplos importantes incluem:
Lactato
Antes visto apenas como resíduo metabólico, o lactato participa da modulação imune e da comunicação celular.
Succcinato
O succinato pode atuar como sinal pró-inflamatório, estabilizando HIF-1α e promovendo produção de IL-1β.
Ácidos graxos de cadeia curta
Produzidos pela microbiota intestinal, especialmente butirato, acetato e propionato, exercem efeitos:
anti-inflamatórios;
epigenéticos;
metabólicos;
imunomoduladores.
Esses compostos ajudam a manter integridade intestinal e tolerância imunológica.
Mitocôndrias: O Centro Integrador
As mitocôndrias assumem papel central nessa nova visão fisiológica.
Além de produzir ATP, elas:
regulam apoptose;
controlam espécies reativas de oxigênio;
participam da sinalização imune;
influenciam inflamação;
modulam envelhecimento celular.
Disfunção mitocondrial está associada a:
fadiga crônica;
doenças neurodegenerativas;
resistência à insulina;
infertilidade;
doenças cardiovasculares;
sarcopenia;
inflamação persistente.
Mitocôndrias também respondem a hormônios como cortisol, hormônios tireoidianos, estrogênio e insulina.
Isso transforma metabolismo energético em um dos principais reguladores da saúde sistêmica.
Microbiota Intestinal e Comunicação Sistêmica
O intestino funciona como uma interface metabólica, imunológica e neuroendócrina.
A microbiota intestinal influencia:
produção de neurotransmissores;
metabolismo estrogênico;
integridade da barreira intestinal;
atividade imune;
metabolismo de ácidos biliares;
inflamação sistêmica.
Disbiose intestinal está associada a:
obesidade;
doenças autoimunes;
depressão;
ansiedade;
resistência à insulina;
doenças neurodegenerativas.
Lipopolissacarídeos bacterianos podem atravessar barreiras intestinais comprometidas e induzir endotoxemia metabólica, promovendo inflamação crônica.
Inflamação Crônica de Baixo Grau
Uma das principais características das doenças modernas é a presença de inflamação crônica subclínica.
Diferente da inflamação aguda, que é protetora, a inflamação persistente de baixo grau gera dano progressivo aos tecidos.
Esse estado inflamatório é alimentado por:
excesso calórico;
sedentarismo;
privação de sono;
estresse crônico;
disbiose;
toxinas ambientais;
hiperinsulinemia;
obesidade visceral.
Citocinas inflamatórias alteram receptores hormonais, prejudicam sinalização da insulina, reduzem conversão tireoidiana e afetam neurotransmissores.
A consequência é uma perda gradual da flexibilidade metabólica e da capacidade adaptativa do organismo.
Neuroimunologia e Eixo Cérebro-Corpo
O cérebro também participa intensamente dessa rede integrada.
Citocinas inflamatórias podem atravessar a barreira hematoencefálica ou sinalizar através do nervo vago, influenciando:
humor;
cognição;
comportamento alimentar;
percepção de dor;
fadiga;
sono.
Neuroinflamação está implicada em:
depressão;
ansiedade;
doença de Alzheimer;
Parkinson;
transtornos metabólicos;
síndrome da fadiga crônica.
Ao mesmo tempo, o cérebro regula imunidade e metabolismo através do sistema nervoso autônomo e do eixo hipotálamo-hipófise-adrenal.
Medicina de Precisão e Individualidade Biológica
A integração entre hormônios, imunidade e metabolismo também reforça a importância da individualidade biológica.
Polimorfismos genéticos, epigenética, microbiota, composição corporal, exposição ambiental e estilo de vida modificam profundamente a resposta fisiológica de cada indivíduo.
Duas pessoas podem apresentar:
respostas inflamatórias diferentes;
sensibilidade distinta à insulina;
metabolismo hormonal variável;
tolerância alimentar desigual;
capacidade antioxidante diferente.
Isso explica por que abordagens padronizadas frequentemente falham em doenças complexas. A fisiologia humana é dinâmica, contextual e adaptativa. Aprenda mais sobre genômica e metabolômica aqui.
Implicações Clínicas
Repensar a fisiologia significa abandonar abordagens reducionistas.
Na prática clínica, isso exige:
avaliação integrada;
compreensão de redes metabólicas;
análise de inflamação sistêmica;
investigação de saúde intestinal;
avaliação hormonal contextualizada;
atenção ao sono, estresse e ritmo circadiano.
Também implica reconhecer que sintomas aparentemente desconectados podem compartilhar mecanismos fisiopatológicos comuns.
Por exemplo:
resistência à insulina pode influenciar fertilidade;
disbiose pode impactar humor e imunidade;
inflamação pode alterar metabolismo hormonal;
privação de sono pode aumentar resistência à insulina e citocinas inflamatórias.
A fisiologia humana não funciona em compartimentos isolados. Hormônios, sistema imune e metabolismo formam uma rede altamente integrada, em constante comunicação. Doenças crônicas modernas emergem justamente da perda dessa integração e da incapacidade adaptativa do organismo diante de estímulos persistentes como excesso calórico, sedentarismo, estresse crônico, inflamação e disfunção mitocondrial.
Repensar a fisiologia significa compreender o corpo como um sistema dinâmico, interdependente e biologicamente inteligente. Essa visão integrada não apenas amplia a compreensão científica da saúde humana, mas também abre caminho para abordagens clínicas mais precisas, preventivas e individualizadas.
No futuro, a medicina tende a abandonar modelos centrados apenas em sintomas e órgãos isolados para adotar uma abordagem sistêmica baseada na interação entre metabolismo, imunidade, neurobiologia e endocrinologia. Essa mudança já começou. Aprenda mais sobre genômica e metabolômica aqui.