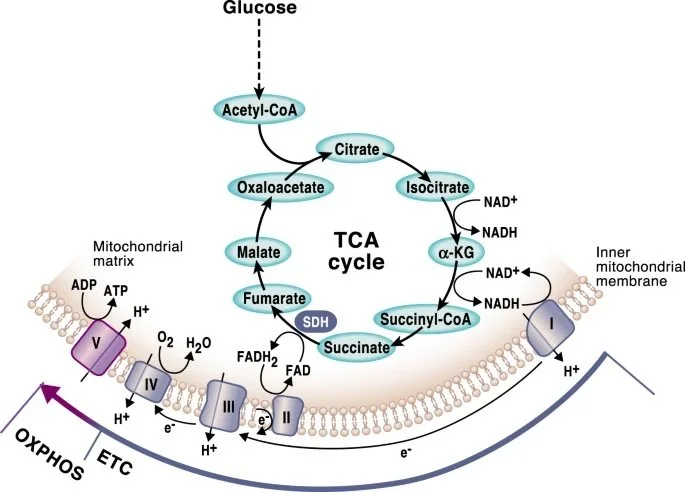
A acetil-CoA é como uma “moeda energética universal” dentro das células. Ela vem do metabolismo de carboidratos, gorduras e proteínas — e alimenta o ciclo de Krebs (também conhecido como ciclo do ácido tricarboxílico), a principal rota de geração de energia nas mitocôndrias.
A acetil-CoA é o intermediário comum da oxidação de carboidratos (via piruvato → piruvato desidrogenase), de ácidos graxos (via β-oxidação) e de certos aminoácidos. Ao entrar no ciclo do TCA (Krebs), a acetil-CoA combina-se com oxaloacetato para formar citrato, permitindo a produção de NADH, FADH₂ e GTP/ATP para alimentar a fosforilação oxidativa.
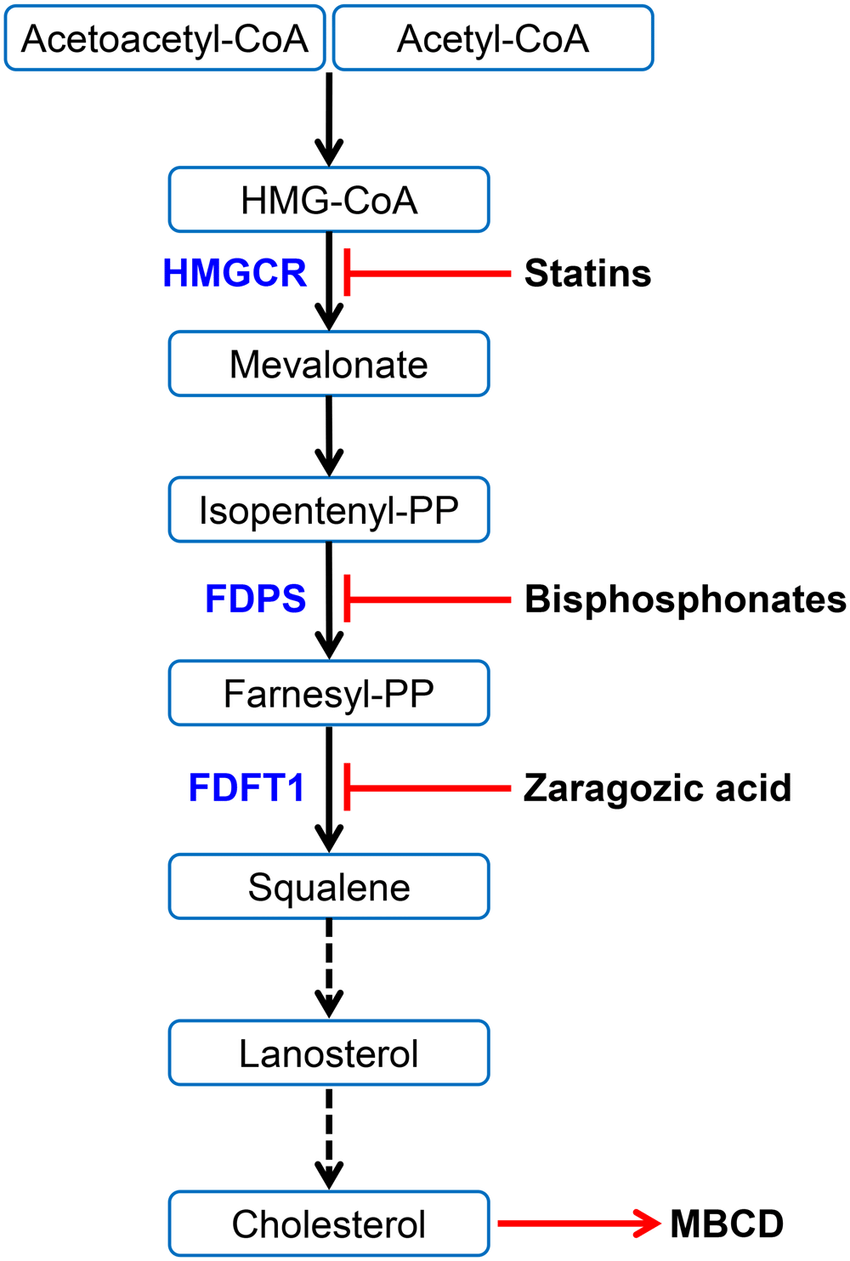
Via do mevalonato: síntese de colesterol e medicamentos que inibem a via (Griffin, Preta, & Sheldon, 2017)
Também atua como precursor para biossíntese lipídica e de colesterol: citrato exportado da mitocôndria pode ser convertido de volta em acetil-CoA no citosol para formar ácidos graxos ou esteróis.
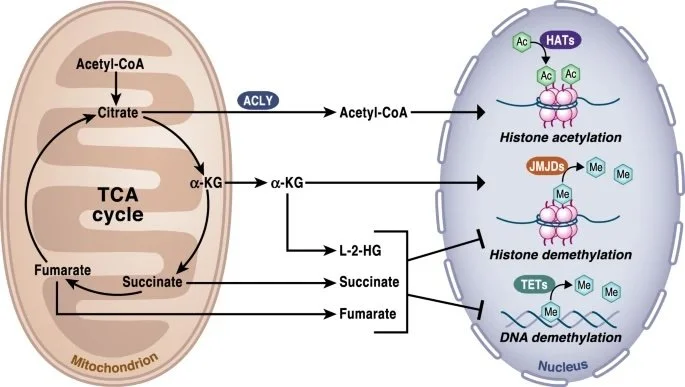
Mas o papel dela vai muito além da geração de energia! A acetil-coA é precursora das enzimas acetiltransferases de lisina (KATs/HATs) que transferem grupos acetil para resíduos de lisina em histonas ou outras proteínas. Isso modula a estrutura da cromatina e a expressão dos genes.
Acetil-CoA e o controle dos genes 🧬
A acetil-CoA atua no núcleo da célula, doando grupos acetil para as histonas — proteínas que enrolam o DNA. Esse processo, chamado acetilação de histonas, “abre” a cromatina e ativa genes ligados a crescimento, diferenciação e defesa celular.
Em termos práticos, isso significa que os níveis de acetil-CoA afetam quais genes “ligam” ou “desligam” sem alterar o DNA em si — um mecanismo de regulação metabólica → epigenética.
Acetil-CoA e imunidade
Durante a ativação de células imunes, como macrófagos e linfócitos, os níveis de acetil-CoA aumentam para reprogramar o metabolismo e ativar genes inflamatórios ou anti-inflamatórios. Ela é literalmente um interruptor entre inflamação e reparo.
Acetil-CoA, longevidade e doenças
Alterações na produção ou uso da acetil-CoA estão ligadas a:
Síndromes metabólicas e resistência à insulina
Doenças neurodegenerativas
Envelhecimento celular
Câncer (por reprogramação epigenética)
Equilíbrio é tudo — tanto o excesso quanto a falta podem ser prejudiciais. Comer muito aumenta a disponibilidade de acetil-CoA e isso contribui, indiretamente, para um ambiente favorável ao desenvolvimento de câncer.
Em células cancerígenas, por exemplo, há evidências de que o enriquecimento (excesso) de acetil-CoA está ligado a agressividade tumoral via estimulação de genes de proliferação (via histona acetilação).
Em células cancerígenas a produção de acetil-CoA está aumentada
A imagem anterior mostra como o aumento ou a desregulação do acetil-CoA pode favorecer o desenvolvimento do câncer, estimulando várias características clássicas das células tumorais:
Sustentar sinalização proliferativa
Evitar supressores de crescimento
Resistir à morte celular
Habilitar imortalidade replicativa
Ativar invasão e metástase
Induzir angiogênese (formação de novos vasos sanguíneos)
Esses processos estão associados a diferentes tipos de câncer (fígado, cérebro, pulmão, pâncreas, mama, cólon, estômago, rins).
Por que os exames metabolômicos são o futuro da medicina?
A metabolômica analisa centenas de metabólitos — como acetil-CoA, succinato, fumarato e itaconato — revelando o que realmente está acontecendo no seu metabolismo em tempo real.
Enquanto os exames tradicionais olham “o resultado” (como glicose ou colesterol), a metabolômica olha os caminhos bioquímicos. Isso permite detectar disfunções antes de surgirem sintomas ou doenças crônicas.
A acetil-CoA é o elo invisível entre o que você come, como você vive e o modo como seus genes se comportam. E a metabolômica é a lupa que permite enxergar esse elo. A análise de metabólitos mitocondriais nos ajuda a entender como a célula gera energia, responde ao estresse e como o tumor pode se adaptar, oferecendo informações valiosas para estratégias terapêuticas personalizadas.
Outros metabólitos associados ao câncer
A metabolômica está revelando insights poderosos sobre o câncer. Ela permite identificar marcadores importantes em pacientes oncológicos, como o p-hidroxifenilactato (associado à proliferação celular) e o 8-hidroxi-2'-desoxiguanosina – 8-OHdG (indicador de dano ao DNA e estresse oxidativo).
O câncer cresce em um ambiente de alto estresse oxidativo, com produção excessiva de radicais livres e antioxidantes. Esse equilíbrio delicado não só favorece a progressão tumoral, mas também influencia tratamentos como quimioterapia e radioterapia, que dependem da oxidação para eliminar células cancerígenas.
⚠️ Atenção com o uso de antioxidantes durante o tratamento oncológico! Eles podem reduzir a eficácia da terapia e até tornar o tumor mais resistente. Não suplemente sem conversar com um profisisonal de saúde habilitado na área.
📊 A metabolômica não serve apenas para diagnóstico precoce, mas também para monitorar a resposta ao tratamento e o risco de recidiva, oferecendo uma visão detalhada do metabolismo tumoral.
Você já conhecia esses marcadores? Compartilhe este post e ajude pacientes e profissionais da saúde a expandirem seu conhecimento sobre essa ferramenta transformadora da medicina de precisão!