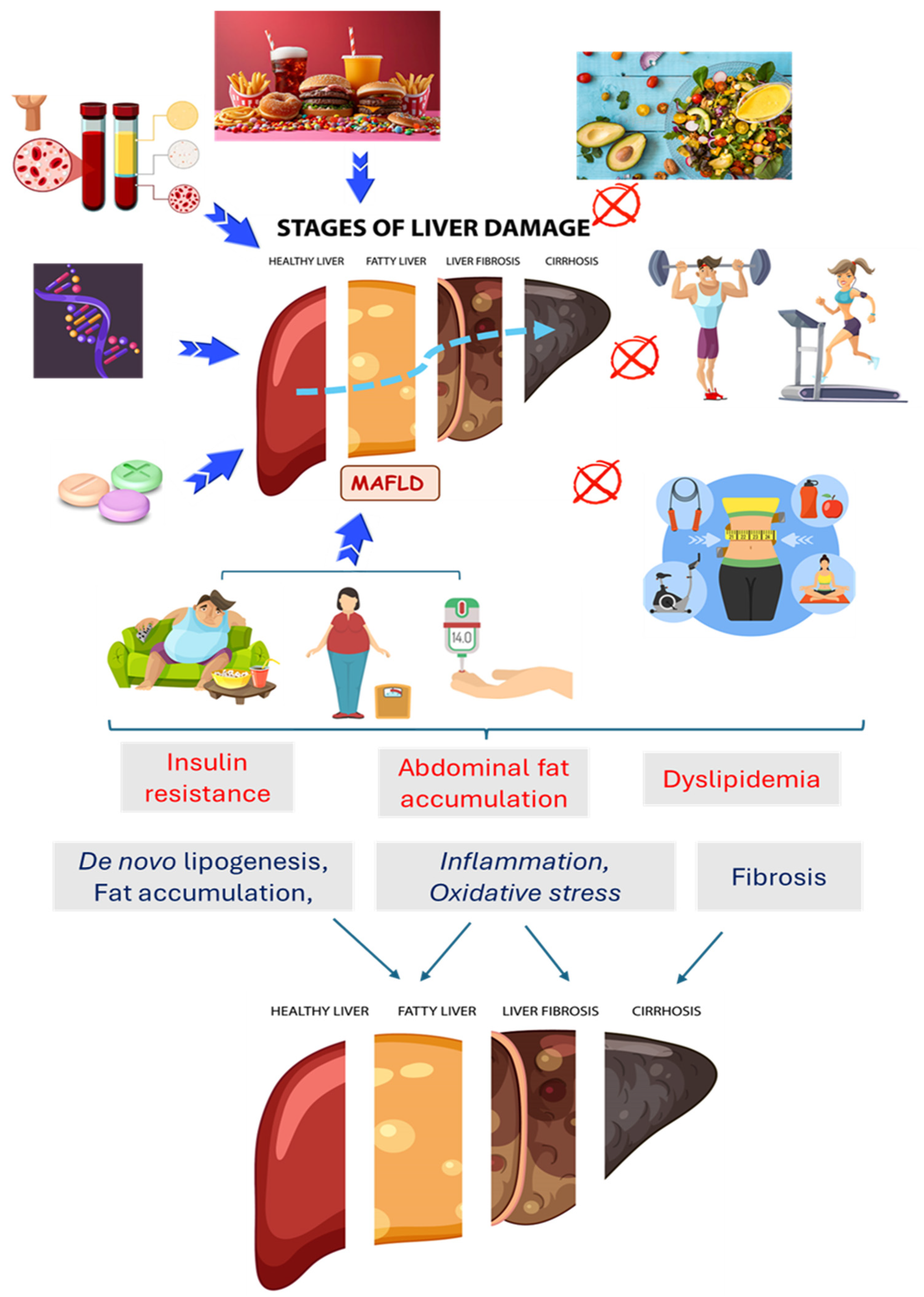
Você já ouviu falar de NAFLD: doença hepática gordurosa não alcoólica? A NAFLD é caracterizada por acumulação de gordura no fígado (esteatose) em ausência de consumo excessivo de álcool, e está associada a resistência à insulina, alteração no metabolismo lipídico e stress oxidativo. Atualmente a sigla NAFLD tem sido substituída por duas outras: MASLD e MASH.
MASLD (Metabolic dysfunction-associated steatotic liver disease). É a fase inicial. Acúmulo de gordura no fígado associado a disfunção metabólica.
MASH (Metabolic dysfunction-associated steatohepatitis). É a progressão inflamatória. Há lesão celular, inflamação e risco de fibrose.
A mudança de nome não é cosmética. Ela reflete o entendimento atual: o problema central não é o álcool ou mesmo a gordura. É a disfunção metabólica.
Antes se pensava assim:
gordura/álcool → inflamação → doença hepática
Hoje o modelo é este:
disfunção metabólica → desequilíbrio redox → alteração enzimática → acúmulo de gordura → inflamação → mais disfunção metabólica
Regulação redox das enzimas no metabolismo lipídico
O fígado desempenha um papel central no metabolismo das gorduras: síntese de ácidos gordos, esterificação em triglicerídeos, oxidação (β‑oxidação) etc. O estado redox (ex: razões NADH/NAD⁺, NADPH/NADP⁺, GSH/GSSG) modula actividade de várias enzimas envolvidas. Por exemplo, excesso de equivalentes redutores (muito NADH) pode suprimir β‑oxidação, favorecer lipogénese.
O estado redox é a relação entre:
NADH / NAD⁺
NADPH / NADP⁺
GSH / GSSG
Isso define:
produção de energia
oxidação de gordura
síntese de gordura
resposta inflamatória
sensibilidade à insulina
Não é detalhe bioquímico. É controle metabólico.
Quando há:
excesso de equivalentes redutores (especialmente NADH)
acontece:
redução da β-oxidação
aumento da lipogênese
aumento de ROS
resistência à insulina
Isso cria o ambiente perfeito para MASLD.
Modificações pós‑translacionais dependentes de redox
O stress oxidativo pode levar a modificações irreversíveis ou semi‑irreversíveis em proteínas (carbonilação, aductos com 4‑HNE, etc) que afectam a função normal das enzimas/metabolismo.
O desequilíbrio redox pode afectar a sensibilidade à insulina. Por exemplo, oxidação de ácido palmítico (vs oleico) leva a aumento de ROS, activação de JNK e inibição da sinalização da insulina.
A acumulação de gorduras no fígado (esteatose) e a resistência à insulina parecem mutuamente relacionadas, mas o mecanismo exacto está ainda por definir — o artigo sugere que o redox desequilibrado pode estar entre os elos de ligação.
Controladores transcricionais / receptores nucleares (NRs) como sensores redox e reguladores do metabolismo lipídico
Receptores nucleares como Peroxisome proliferator-activated receptors (PPAR α/γ/δ), Sterol regulatory element-binding proteins (SREBP), AMP-activated protein kinase (AMPK), Liver X receptors (LXR) e Farnesoid X receptor (FXR) surgem como choke‑points: regulam síntese/oxidação lipídica e são influenciados por ligandos lipídicos, mas também pelo estado redox.
Exemplo: H₂O₂ diminui a expressão de PPARα/γ (reduzindo β‑oxidação) e activa SREBP1c (aumentando lipogênese).
Portanto, os receptores nucleares podem actuar como sensores redox/metabólicos — transformando sinais de stress oxidativo em alterações no metabolismo lipídico.
Hoje, os principais alvos terapêuticos em MASLD/MASH são:
PPAR (α, γ, δ)
FXR
THR-β (receptor de hormona tiroideia)
AMPK
Esses receptores controlam:
oxidação de gordura
inflamação
sensibilidade à insulina
fibrose
E todos são regulados por estado redox. Estudos recentes mostram isso de forma direta:
Receptores nucleares regulam metabolismo lipídico, glicose, inflamação e fibrose, sendo considerados alvos terapêuticos promissores em MASLD.
Agonistas de PPAR estão em ensaios clínicos e demonstram melhora metabólica e hepática em pacientes com doença hepática metabólica.
Em 2024, foi aprovado o primeiro medicamento específico para MASH: o Resmetirom.
Mecanismo:
ativa THR-β
aumenta oxidação de ácidos gordos
reduz gordura hepática
Resultados:
cerca de 26 a 30% dos pacientes tiveram resolução da inflamação hepática em 52 semanas, versus cerca de 10% no placebo (Zhou et al., 2025).
Isso é uma prova clínica de conceito: modular receptores nucleares funciona
Defesas antioxidantes, terapêutica e implicações clínicas
O fígado possui mecanismos antioxidantes (ex: SOD, catalase, glutationa) que ficam comprometidos nas doenças do fígado. A acumulação de colesterol livre, por exemplo, pode esgotar a glutationa mitocondrial e predispor a lesão hepática.
Reforçar as defesas antioxidantes ou modular os receptores nucleares/vias metabólicas redox‑dependentes aparece como alvo promissor para cuidados como fígado (Tauil et al., 2024).
Estudos mostram que compostos antioxidantes:
reduzem inflamação
melhoram função mitocondrial
modulam expressão génica metabólica
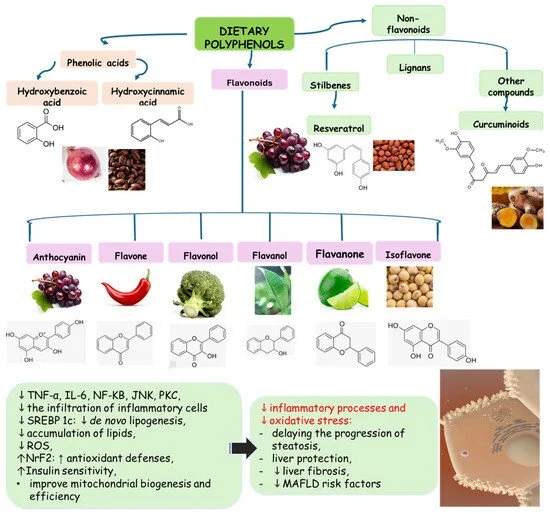
Especialmente polifenóis, flavonoides, compostos fenólicos dos alimentos, que atuam em:
PPAR
NF-κB
AMPK
Nrf2
Os fitocompostos podem atuar como compostos preventivos ou podem fornecer tratamento natural e complementar os tratamentos existentes para MAFLD e outras doenças hepáticas, como a esteatose. Os resultados dos ensaios clínicos incluídos mostram que esses compostos, em comparação com o placebo, podem alcançar o seguinte:
Reduzir o peso corporal, o IMC, a circunferência da cintura, os índices de gordura visceral e a massa de gordura abdominal visceral e subcutânea;
Diminuir o colesterol total plasmático, os triglicerídeos e o LDL-c;
Reduz as concentrações plasmáticas de LDL-c oxidado aterogênico;
Reduz a hemoglobina glicada, a glicemia, a resistência à insulina e o índice HOMA;
Reduz os níveis plasmáticos de leptina (bem como a relação leptina-adiponectina);
Reduz a excreção urinária de 8-isoprostano;
Reduz a indução de NF-κB;
Reduz os níveis séricos de citoqueratina-18 e kisspeptina;
Reduz os níveis de interleucinas pró-inflamatórias, como IL-1β, IL-6, IL-18 e TNF-α;
Diminui a expressão de mRNA do inflamassoma NLRP3 (caspase-1, IL-1β e IL-18) em células mononucleares do sangue periférico;
Reduz a pressão arterial sistólica e diastólica;
Melhora os níveis de HDL-c e adiponectina;
Melhorar a relação de atenuação entre fígado e baço na tomografia computadorizada;
Melhorar a dilatação mediada pelo fluxo e a espessura da íntima-média da carótida;
Diminuir o conteúdo de gordura hepática, o índice de esteatose e o nível de fibrose;
Melhorar os marcadores de fibrogênese.
Reduzir significativamente gama-GT, AST e ALT;