A lactilação é uma modificação pós-traducional dependente do metabolismo que liga diretamente a glicólise à regulação transcricional.
1. Origem metabólica
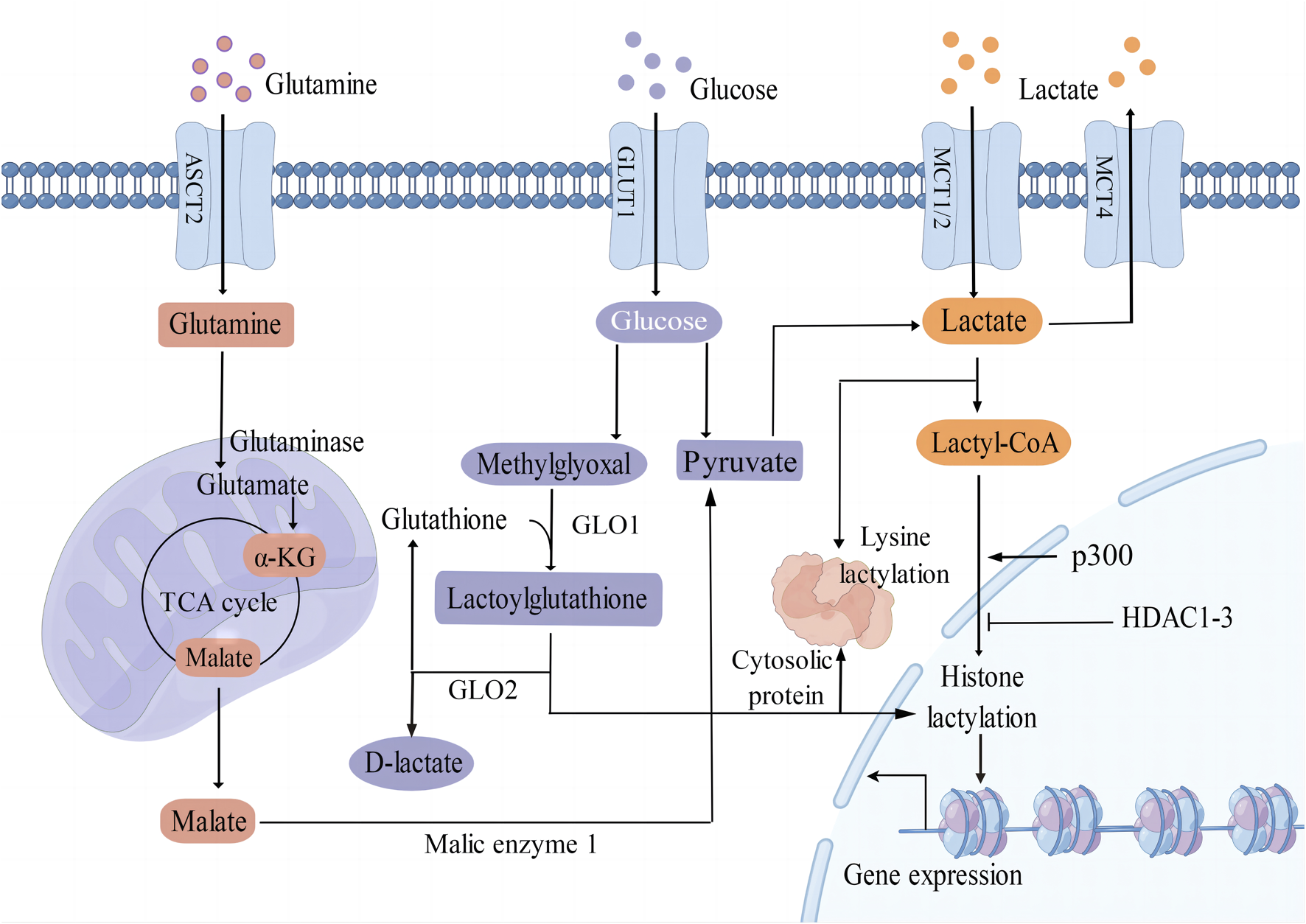
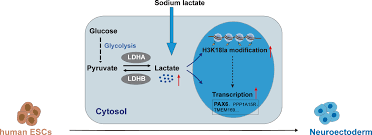
A glicólise converte glicose em piruvato, posteriormente reduzido a lactato via LDH.
O lactato intracelular acumula-se em condições de alta taxa glicolítica ou hipóxia.
Esse lactato atua como precursor de grupos lactil (lactil-CoA ou vias intermediárias como lactoilglutationa).
Neste caso, o lactato deixa de ser resíduo metabólico e passa a sinalizador epigenético.
2. Reação de lactilação
O grupo lactil é adicionado covalentemente a resíduos de lisina em histonas e proteínas não histônicas.
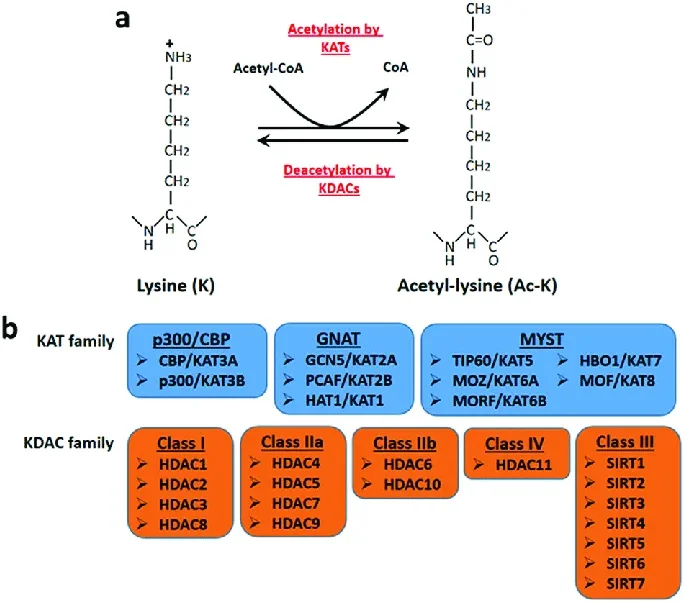
Enzimas “writers” como p300 catalisam a transferência; “erasers” (ex. HDAC1–3) removem a modificação.
Resultado molecular: formação de marcas como H3K18la e H3K23la.
3. Efeito sobre a cromatina
A lactilação altera a carga da lisina → reduz interação histona-DNA.
Promove maior acessibilidade da cromatina em regiões regulatórias.
Ativa enhancers e promotores gênicos.
Consequência: favorece um estado transcricional permissivo.
4. Regulação da expressão gênica
Aumenta expressão de genes associados a:
metabolismo glicolítico
diferenciação celular
resposta inflamatória e adaptação hipóxica
Atua como sensor metabólico, acoplando disponibilidade energética à transcrição.
5. Integração metabolismo–epigenoma
Fluxo glicolítico elevado → ↑ lactato → ↑ lactilação → reprogramação gênica
Cria loops positivos em estados como:
diferenciação celular
tumorigênese
resposta imune
A lactilação funciona como nó integrador entre metabolismo, cromatina e sinalização celular.
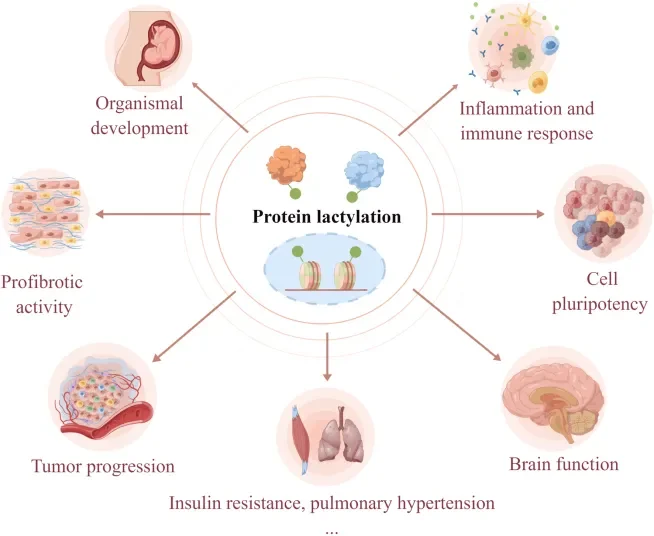
6. Implicações biológicas
Desenvolvimento embrionário e plasticidade celular
Polarização de macrófagos e imunomodulação
Progressão tumoral e resistência terapêutica
A lactilação é um mecanismo epigenético dependente de lactato que traduz o estado metabólico da célula em alterações estruturais da cromatina, modulando diretamente a expressão gênica e permitindo adaptação funcional em contextos fisiológicos e patológicos.