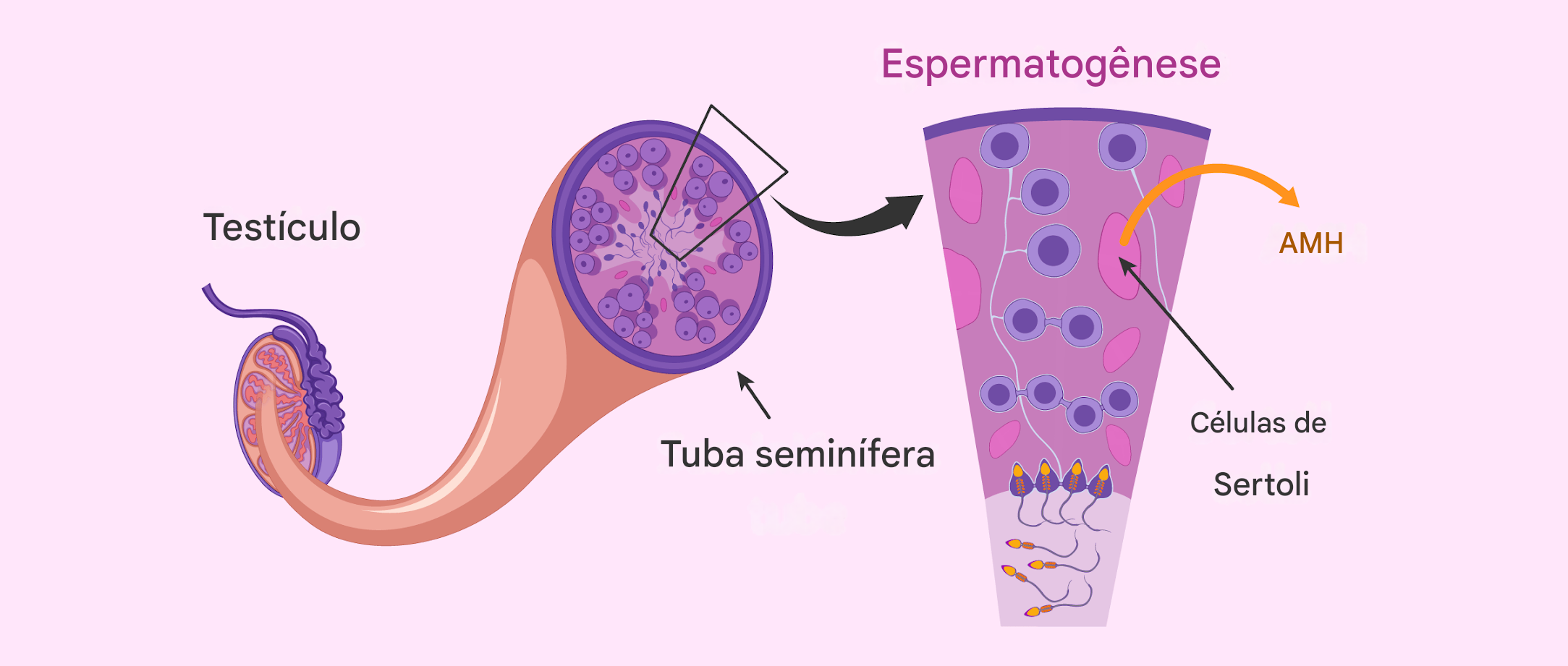
O hormônio anti-Mülleriano (AMH) é produzido pelas células de Sertoli, que ficam dentro dos testículos. Essas células são essenciais para a formação e a manutenção dos espermatozóides.
Durante a vida fetal, o AMH indica que os testículos estão se desenvolvendo corretamente. Além disso, a quantidade de células de Sertoli formada nesse período influencia diretamente o número de células germinativas na vida adulta, ou seja, a capacidade futura de produzir espermatozoides.
Na vida adulta, o AMH continua sendo um marcador importante da função testicular, especialmente da atividade das células de Sertoli. Por isso, vem sendo cada vez mais estudado em casos de infertilidade masculina.
Regulação hormonal do AMH
O hormônio folículo-estimulante, FSH, estimula a produção de AMH quando não há forte ação de hormônios androgênicos. Já a testosterona exerce efeito contrário, reduzindo a produção de AMH. Isso significa que existe um equilíbrio entre FSH e testosterona controlando os níveis de AMH.
AMH indetectável e testosterona baixa - Sugere ausência ou falência grave do tecido testicular funcional, como pode ocorrer na Síndrome de Klinefelter em sua forma mais severa, quando há prejuízo importante da espermatogênese.
Testosterona normal e AMH indetectável - É fortemente sugestivo de Síndrome do ducto de Müller persistente, especialmente quando associado a sinais clínicos compatíveis. Nessa condição, há alteração específica na ação do AMH durante o desenvolvimento fetal.
AMH e testosterona abaixo do normal - Ocorre em distúrbios mistos do desenvolvimento sexual, conhecidos como DDS misto. Nesse quadro, há disfunção tanto das células de Leydig, responsáveis pela produção de testosterona, quanto das células de Sertoli, comprometendo o desenvolvimento sexual desde o período fetal.
AMH em outras condições relacionadas à fertilidade masculina
Os níveis de AMH podem variar em diferentes situações clínicas, como:
Atraso puberal
Hipogonadismo hipogonadotrópico congênito grave
Azoospermia não obstrutiva
Síndrome de Klinefelter
Varicocele
Síndrome de McCune-Albright
Senescência masculina
AMH e avaliação da azoospermia
A azoospermia é a ausência de espermatozoides no sêmen. Ela pode ser:
Obstrutiva, quando há produção normal de espermatozoides, mas existe bloqueio no trajeto.
Não obstrutiva, quando o problema está na própria produção testicular.
Estudos mostram que o AMH pode ser utilizado como marcador indireto da espermatogênese. Quando analisado isoladamente ou em conjunto com o FSH, pode auxiliar na diferenciação entre azoospermia obstrutiva e não obstrutiva.