O corpo humano abriga bilhões de microrganismos, como bactérias, fungos, vírus e protozoários, que formam a microbiota. Esses microrganismos, junto com seus genes, conhecidos como microbioma, desempenham funções essenciais para a nossa sobrevivência. Particularmente, a microbiota intestinal é composta por mais de 10⁴ microrganismos de 300 a 3000 espécies, codificando 200 vezes o número de genes humanos.
A microbiota intestinal é vital para várias funções biológicas, incluindo a absorção de nutrientes, como carboidratos, proteínas, ácidos biliares e vitaminas. Além disso, ela impacta funções não gastrointestinais, como o desenvolvimento do cérebro e a maturação dos sistemas imunológico e neuroendócrino, com efeitos que começam ainda no período embrionário e se estabelecem de forma irreversível em fases críticas do desenvolvimento.
A Relação Bidirecional entre o Microbioma e o Hospedeiro
A relação entre o microbioma intestinal e seu hospedeiro é bidirecional. Fatores como dieta, saúde e estilo de vida influenciam a composição do microbioma intestinal, assim como mudanças modernas na alimentação e o aumento das cesáreas impactam essa composição. Além disso, os avanços médicos e tratamentos farmacológicos também desempenham um papel relevante nessa dinâmica.
A mudança no padrão de doenças humanas, com um aumento de doenças autoimunes, cardiovasculares, metabólicas e mentais, tem sido associada a desequilíbrios no microbioma intestinal. Doenças como asma, diabetes, depressão, ansiedade e distúrbios neurológicos como TDAH e autismo, estão ligadas a essas alterações.
Microbioma Intestinal e o Eixo Intestino-Cérebro
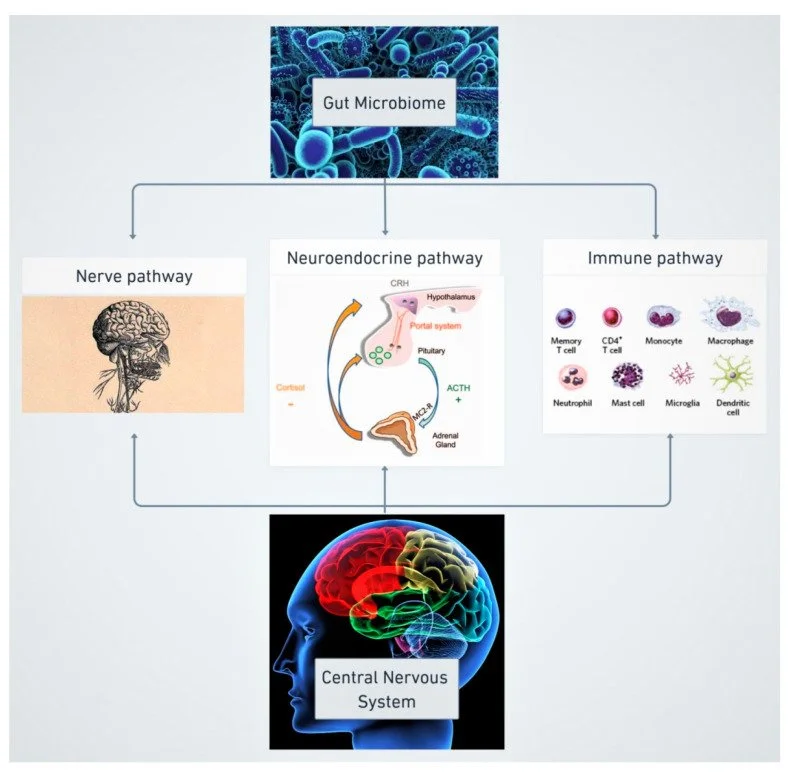
O termo "eixo intestino-cérebro" descreve a comunicação bidirecional entre o microbioma intestinal e o sistema nervoso central (SNC). Essa interação ocorre por meio de três vias principais: nervosa, neuroendócrina e imunológica. O nervo vago, principal responsável pela via nervosa, desempenha um papel essencial na regulação do humor, sendo ativado por metabólitos microbianos.
Essa comunicação entre intestino e cérebro tem implicações importantes no comportamento e nas respostas emocionais, com estudos mostrando que infecções intestinais podem alterar o comportamento e a resposta ao estresse.
Estudos recentes têm mostrado que o microbioma intestinal desempenha um papel crucial no comportamento e na saúde mental. Por exemplo, o Lactobacillus rhamnosus e o Bifidobacterium longum demonstraram aliviar sintomas de ansiedade e depressão em modelos experimentais. Além disso, pesquisas sobre o Lactobacillus reuteri indicam que os efeitos comportamentais relacionados ao autismo podem ser alterados em camundongos vagotomizados, sugerindo a importância da comunicação entre o intestino e o cérebro.
Eixo Microbiota-Intestino-Cérebro e Transtorno de Déficit de Atenção e/ou Hiperatividade (TDAH)
O microbioma intestinal tem grande influência na fisiopatologia de transtornos como o TDAH, afetando o comportamento e o desenvolvimento neuropsicológico. A modulação do microbioma pode, assim, oferecer novos caminhos terapêuticos para condições como o TDAH, especialmente em pacientes pediátricos.
O TDAH é o transtorno neuropsiquiátrico mais comum na infância, afetando 5% das crianças e adolescentes. Caracteriza-se por desatenção, hiperatividade e impulsividade, com sintomas que frequentemente persistem na vida adulta em 40-60% dos casos. Este transtorno impacta várias áreas, incluindo saúde física, desempenho acadêmico e social. O tratamento primário envolve psicoestimulantes, como o metilfenidato, que aumentam os níveis de neurotransmissores como dopamina (DA) e norepinefrina (NE), mas o uso prolongado pode ser limitado por efeitos adversos e resistência social à medicação.
Diversos fatores contribuem para o TDAH, incluindo fatores genéticos (70-80%) e ambientais, como prematuridade e negligência infantil. A fisiopatologia do TDAH está associada a déficits nas funções executivas e alterações neuroanatômicas, particularmente no córtex pré-frontal. Além disso, a disfunção do sistema mesolímbico dopaminérgico e a alteração na neurotransmissão catecolaminérgica têm sido indicadas como possíveis causas do transtorno.
Há também evidências de que o estresse oxidativo e a inflamação desempenham papéis importantes no TDAH, exacerbando as alterações neuroquímicas. Estudos indicam níveis elevados de marcadores de estresse oxidativo e danos mitocondriais, especialmente nos neurônios dopaminérgicos. A ativação da microglia e a liberação de citocinas inflamatórias também podem contribuir para a progressão do TDAH, criando um ciclo vicioso de inflamação e danos neuronais.
Perfis Microbianos Intestinais e TDAH: Associação com Sintomas e Implicações Fisiopatológicas
A composição microbiana intestinal tem atraído crescente interesse como possível fator contribuinte para o Transtorno de Déficit de Atenção e Hiperatividade (TDAH). Diversos estudos sugerem que o microbioma intestinal de indivíduos com TDAH pode diferir significativamente daqueles sem o transtorno, refletindo potenciais implicações nas vias metabólicas e nos sintomas do TDAH.
Aarts et al. (2017) - Microbioma e Recompensa Neural Aarts e colaboradores foram pioneiros ao relatar diferenças na composição microbiana intestinal de pacientes com TDAH. Utilizando sequenciamento de última geração, eles observaram um aumento no gênero Bifidobacterium em pacientes com TDAH, correlacionado com a síntese de dopamina. Além disso, uma análise funcional de ressonância magnética mostrou uma associação entre a abundância de Bifidobacterium e respostas alteradas de antecipação de recompensa no cérebro, uma característica frequentemente associada ao TDAH. Embora esse estudo tenha sido inovador, limitações como a diferença de idades entre os grupos e o tamanho da amostra sugerem cautela na interpretação dos resultados.
Jiang et al. (2018) - Efeito de Faecalibacterium Jiang e colegas investigaram a composição microbiana em crianças com TDAH não tratadas com medicação, encontrando uma redução no gênero Faecalibacterium associado a sintomas do TDAH. O estudo também apontou que níveis baixos de Faecalibacterium são comumente encontrados em doenças atópicas, como asma, frequentemente associadas ao TDAH. Apesar de não poderem estabelecer causalidade, os autores destacaram a robustez do estudo ao controlar fatores como uso de probióticos e antibióticos, além de sintomas gastrointestinais e psicológicos.
Szopinska-Tokov et al. (2020) - Gênero Ruminococcaceae_UGC_004 Em um estudo com adolescentes com TDAH, Szopinska-Tokov e sua equipe descobriram um aumento no gênero Ruminococcaceae_UGC_004, associado a sintomas de desatenção. Eles sugeriram que esse gênero pode estar relacionado à modulação do neurotransmissor GABA. Embora o estudo tenha revelado conexões entre microbioma e neurotransmissores, as limitações incluem falta de dados sobre o processo de recrutamento das amostras e a ingestão de medicamentos.
Prehn-Kristensen et al. (2021) - Diversidade Microbiana e Hiperatividade Um estudo de Prehn-Kristensen et al. identificou diferenças significativas na diversidade microbiana entre adolescentes com TDAH e controles. A redução da diversidade alfa em pacientes com TDAH foi associada à hiperatividade. Além disso, um aumento da família Bacteroidaceae foi encontrado no grupo com TDAH. A descoberta de uma possível transmissão vertical de características microbianas, como a alteração observada no microbioma das mães, destacou um possível fator hereditário, embora o pequeno tamanho da amostra tenha sido uma limitação importante.
Wan et al. (2021) - Alterações no Microbioma e TDAH em Crianças Um estudo com uma amostra pediátrica chinesa revelou que Faecalibacterium, um gênero anti-inflamatório, estava significativamente reduzido em crianças com TDAH, enquanto outros gêneros como Enterococcus e Odoribacter estavam mais presentes. Essas alterações sugerem que os padrões microbianos podem influenciar a patogênese do TDAH, principalmente por meio de vias dopaminérgicas e inflamatórias. No entanto, o pequeno tamanho da amostra e a falta de informações sobre a medicação foram limitações do estudo.
Casas et al. (2020) - Diversidade Microbiana na Infância e TDAH Casas e colaboradores investigaram a influência da diversidade microbiana no início da vida no desenvolvimento de sintomas de hiperatividade/desatenção. O estudo indicou que a diversidade bacteriana aos 10 anos estava inversamente relacionada ao desenvolvimento de TDAH, enquanto a diversidade fúngica se associava positivamente à prevalência do transtorno. Contudo, como o estudo foi observacional e não considerou outros fatores de confusão, a causalidade não pode ser estabelecida.
Estudo de Stevens et al. (2019) - Realizado com 17 crianças do sexo masculino com TDAH, o estudo duplo-cego controlado por placebo investigou o impacto da suplementação de micronutrientes no microbioma fecal. Após 10 semanas, os participantes que tomaram os micronutrientes apresentaram uma taxa de resposta de 50%, em comparação com 29% no grupo placebo. Embora não houvesse diferenças significativas nas escalas de avaliação de sintomas de TDAH, foi observada uma diminuição significativa no filo Actinobacterium, especialmente no gênero Bifidobacterium, e um aumento no gênero Collinsella. Essas mudanças foram associadas a melhorias no comportamento, como atenção e regulação emocional. No entanto, o estudo apresentou limitações, como uma amostra pequena e a ausência de informações sobre uso de medicamentos.
Estudo de Wang et al. (2019) - Um estudo taiwanês comparou a microbiota fecal e os padrões alimentares entre 30 crianças com TDAH e 30 controles saudáveis. As crianças com TDAH apresentaram uma maior diversidade alfa, mas não diferenças significativas na diversidade beta. Alguns gêneros bacterianos, como Bacteroides e Sutterella, estavam mais abundantes no grupo com TDAH, enquanto Lactobacillus foi mais presente no grupo controle. Além disso, os padrões alimentares diferiram entre os grupos, com as crianças com TDAH consumindo mais grãos refinados e menos laticínios.
Estudo de Cheng et al. (2019) - Este estudo utilizou uma análise de enriquecimento genético (GSEA) para examinar a relação entre o microbioma intestinal e cinco transtornos neuropsiquiátricos, incluindo TDAH. O estudo revelou que o gênero Desulfovibrio e a ordem Clostridiales estavam associados ao TDAH. No entanto, Desulfovibrio também foi associado ao Transtorno do Espectro Autista (TEA), o que sugere que essa associação não é exclusiva do TDAH. A principal inovação deste estudo foi o uso de dados genômicos, tornando os resultados menos influenciados por fatores ambientais.
Embora os estudos mostrem uma relação entre o microbioma intestinal e os sintomas de TDAH, as evidências ainda são inconclusivas. Fatores como características demográficas, geográficas, alimentares e metodológicas, além do uso de medicamentos, podem influenciar os resultados. Mesmo assim, muitos pesquisadores acreditam na hipótese de que a alteração da composição bacteriana pode influenciar vias neurobiológicas, como a neurotransmissão e a neuroinflamação, e contribuir para exacerbação dos sintomas do TDAH.
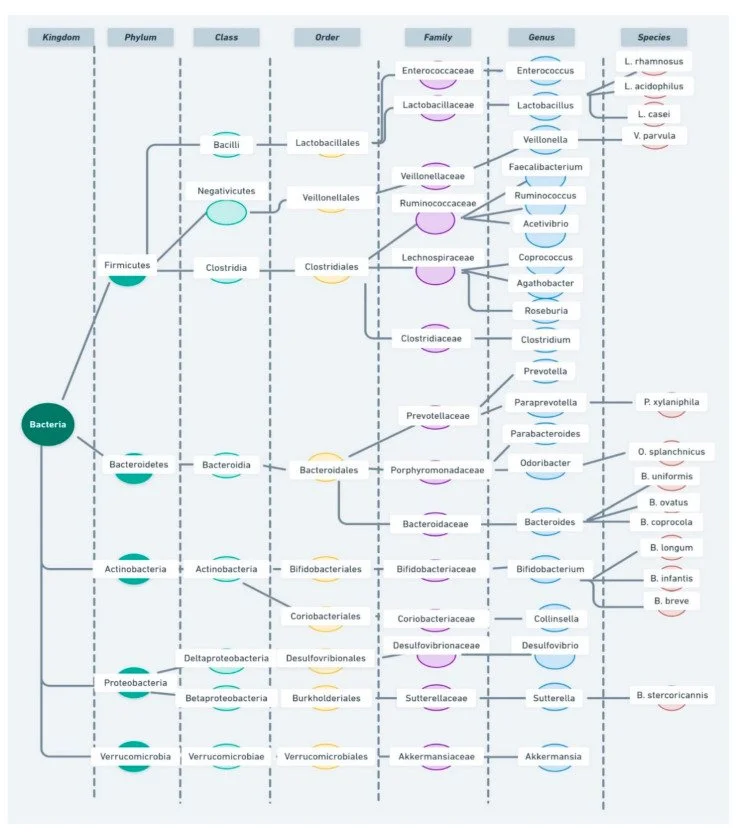
Classificação taxonômica bacteriana, de acordo com o National Center for Biotechnology Information (NCBI) Taxonomy Database Checa-Ros et al., 2021
Microbioma Intestinal e Ácidos Graxos Poli-insaturados Ômega-3 no TDAH
Os ácidos graxos poli-insaturados (PUFAs) ômega-3, especialmente o ácido docosahexaenoico (DHA) e o ácido eicosapentaenoico (EPA), desempenham papéis cruciais na fluidez das membranas celulares, na neurotransmissão e na função dos receptores cerebrais. Eles também influenciam a produção de fatores neurotróficos, como o BDNF (fator neurotrófico derivado do cérebro) e o GDNF (fator neurotrófico derivado de células gliais), que são essenciais para a função dos neurônios dopaminérgicos. A deficiência de DHA no cérebro durante o desenvolvimento pode estar associada à hipofunção dopaminérgica, o que pode impactar condições como o TDAH.
Estudos em modelos animais demonstraram que uma dieta enriquecida com PUFAs ômega-3 pode melhorar sintomas de TDAH, como aumento da atenção e redução da impulsividade. Além disso, os PUFAs ômega-3 possuem propriedades anti-inflamatórias, sendo capazes de reduzir os níveis de interleucinas pró-inflamatórias e inibir a ativação do inflamossoma NLRP3, fatores relacionados a processos inflamatórios no cérebro.
Em pacientes pediátricos com TDAH, observa-se uma proporção maior de ácidos graxos ômega-6 em relação ao ômega-3, sugerindo um desbalanço que pode ser relevante para os sintomas do transtorno. Embora os estudos sobre a suplementação com ômega-3 apresentem resultados mistos, há indícios de que o DHA e o EPA podem contribuir para a melhoria dos sintomas de desatenção e hiperatividade.
Além disso, há um crescente interesse na interação entre os PUFAs ômega-3 e o microbioma intestinal. Experimentos em camundongos demonstraram que a suplementação com diferentes cepas de Bifidobacterium breve alterou os perfis de ácidos graxos nos tecidos, como o aumento das concentrações de DHA no cérebro. Essas mudanças foram acompanhadas por modificações na composição microbiana intestinal, com maior abundância de Clostridiaceae e menor presença de Eubacterium nos grupos suplementados com B. breve.
Estudos com camundongos alimentados com dietas deficientes ou enriquecidas com ômega-3 revelaram mudanças significativas na composição microbiana. Por exemplo, os animais que consumiram uma dieta enriquecida com ômega-3 apresentaram um aumento nos gêneros Lactobacillus e Bifidobacterium, que são conhecidos por sua ação benéfica sobre a saúde intestinal.
Estudos humanos também corroboram essa interação. Em um ensaio com 22 voluntários saudáveis, a suplementação com PUFAs ômega-3 levou ao aumento de Bifidobacterium, Roseburia e Lactobacillus em amostras fecais. No entanto, não houve correlação significativa entre as mudanças microbianas e os níveis de EPA/DHA no sangue, sugerindo que os efeitos microbianos podem ser mais complexos.
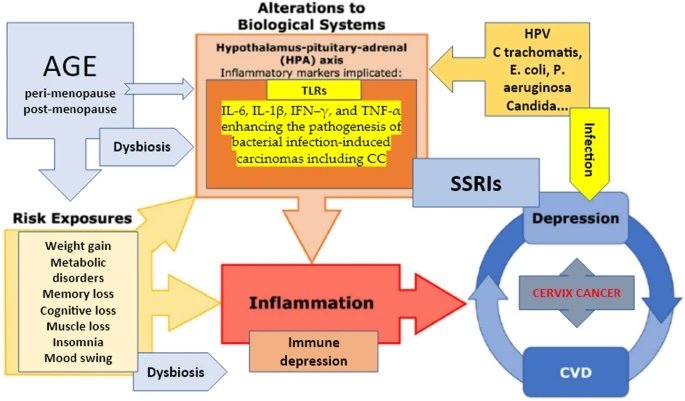
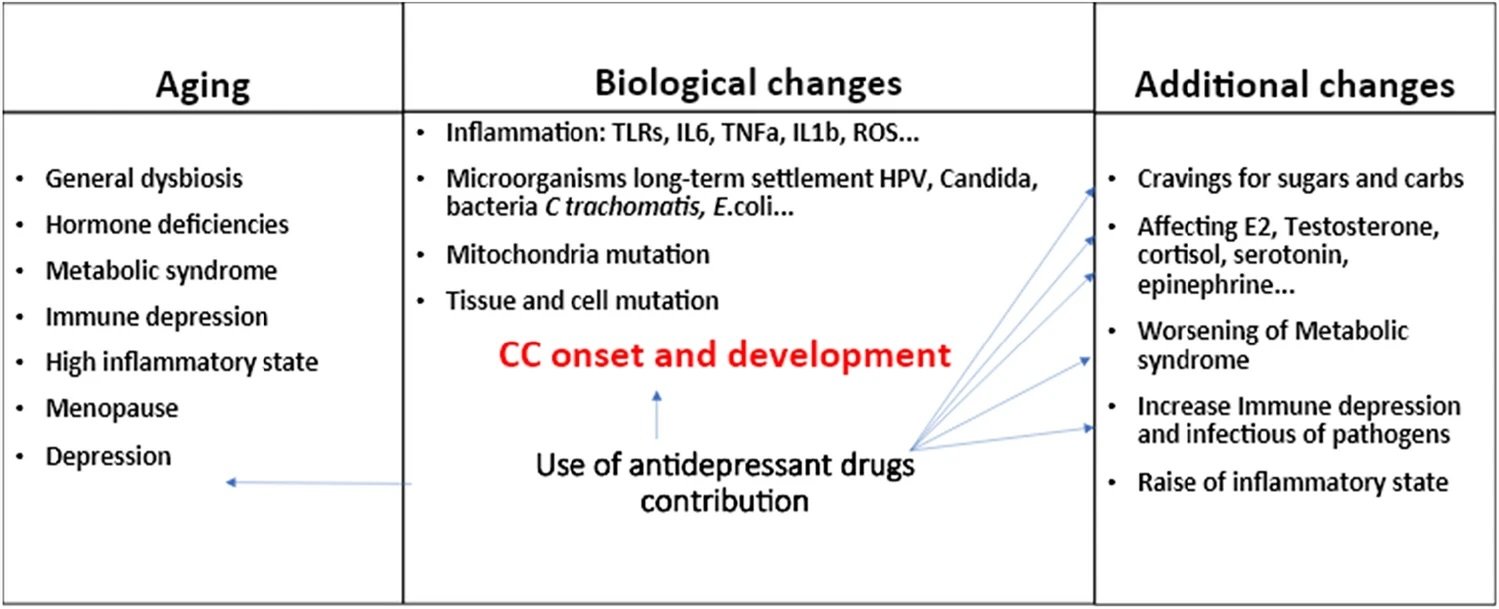
Representação da interação entre o microbioma intestinal e os PUFAs ômega-3 e como essa relação pode interferir nos mecanismos fisiopatológicos do TDAH. Checa-Ros et al., 2021
Proporção Ômega-6:Ômega-3 e o Efeito nos Sintomas do TDAH
Estudos indicam que um desequilíbrio na proporção entre os ácidos graxos ômega-3 e ômega-6 pode levar a um estado de neuroinflamação, resultando em disfunção do sistema dopaminérgico. Esse desequilíbrio (representado por setas pretas na figura acima) é considerado um dos principais fatores que contribuem para os sintomas do TDAH, como impulsividade, desatenção e hiperatividade. Além disso, alterações na composição microbiana intestinal também têm sido associadas aos sintomas do TDAH. O microbioma intestinal influencia a neurotransmissão através do eixo microbioma-intestino-cérebro (MGBA), impactando diretamente a função cerebral e, consequentemente, os sintomas do transtorno.
Uma possível intervenção seria a redução no consumo de óleos vegetais ricos em ômega-6, como soja, milho, girassol, canola, com administração de ômega-3 e suplementação de probióticos, para ajudar a aumentar as concentrações de PUFAs ômega-3 no organismo. Isso ajudaria a corrigir o desequilíbrio entre ômega-3 e ômega-6, promovendo a estabilização das membranas neuronais, a melhora na neurotransmissão dopaminérgica e a redução da neuroinflamação, o que pode levar a uma melhora dos sintomas do TDAH.
Por outro lado, a suplementação direta com ácidos eicosapentaenoico (EPA) e docosahexaenoico (DHA) (seta amarela na figura acima) também pode induzir mudanças benéficas na composição microbiana intestinal. Esses efeitos seriam mediadores da regulação da neurotransmissão dopaminérgica, proporcionando um alívio adicional para os sintomas do TDAH por meio da modulação do MGBA.
Futuras pesquisas devem focar na padronização das dosagens e combinações de probióticos, além de explorar o impacto dos probióticos em comorbidades associadas ao TDAH, como distúrbios do sono. Com a evolução desses estudos, é possível que o microbioma intestinal venha a ser uma nova ferramenta terapêutica no manejo do TDAH, promovendo alternativas eficazes para o tratamento dessa condição em populações pediátricas.