O receptor NMDA (N-metill-d-aspartato) é um tipo de receptor de glutamato ionotrópico acoplado à proteína G que desempenha um papel crucial na regulação de uma ampla variedade de funções neurológicas, incluindo respiração, locomoção, aprendizado, formação de memória e neuroplasticidade.
Consequentemente, o comprometimento estrutural e funcional do receptor NMDA pode levar a distúrbios neurodegenerativos e cognitivos, incluindo doença de Alzheimer, doença de Parkinson, doença de Huntington, dor neuropática, epilepsia e distúrbios psiquiátricos.
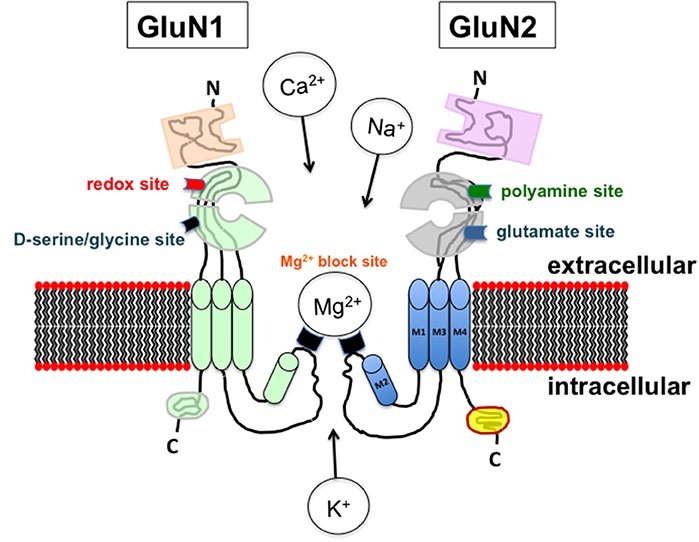
Os receptores NMDA requerem dois ligantes, glutamato e glicina, para ativação. Além disso, os receptores sofrem bloqueio dependente de voltagem pelo Mg2+ e apresentam alta permeabilidade ao Ca2+ quando o bloqueio do Mg2+ é removido.
Estrutura dos receptores NMDA
Os receptores NMDA são compostos por quatro subunidades distintas: duas subunidades GluN1 de ligação à glicina e duas subunidades GluN2 de ligação ao glutamato. Essas subunidades formam um canal central permeável a cátions.
Como qualquer outro receptor, os receptores NMDA sofrem uma alteração conformacional induzida pelo ligante para serem ativados. O glutamato é liberado do terminal pré-sináptico para a fenda sináptica em uma concentração muito alta (cerca de 1,1 mM) e liga-se aos receptores NMDA pós-sinápticos para induzir a abertura dos poros do canal. Leia sobre as funções do glutamato no cérebro neste outro artigo.
Após a ativação, os receptores NMDA continuam a passar correntes pós-sinápticas excitatórias por dezenas a centenas de milissegundos, mesmo após a remoção do glutamato da fenda sináptica. No estado de repouso, o Mg2+ extracelular entra no poro do receptor e liga-se firmemente ao receptor, o que restringe a entrada adicional de íons e impede a ativação do receptor. Após uma despolarização suficientemente forte, o Mg2+ é removido do poro, permitindo a entrada de íons permeantes (Ca2+).
Funções dos receptores NMDA
Os receptores NMDA desempenham papéis cruciais em muitas funções neurológicas:
Regulam a plasticidade estrutural e funcional das sinapses, dendritos e neurônios ativando uma série de vias de sinalização mediadas pelo cálcio.
Fortalecem sinapses, processo conhecido como potenciação de longo prazo (LTP), muito importante para a formação da memória, especialmente na região CA1 do hipocampo. Para uma LTP eficaz, é necessário o influxo de cálcio através do receptor NMDA. O cálcio que entra no receptor induz a ativação da proteína quinase II dependente de cálcio/calmodulina, que por sua vez interage com o receptor NMDA e, assim, aproxima-se do receptor AMPA, levando à fosforilação do receptor AMPA e iniciação de LTP.
Desativação do receptor NMDA
A depressão de longo prazo (DLP) é um fenômeno oposto ao LTP que causa enfraquecimento das sinapses. Mecanicamente, os receptores NMDA medeiam o DLP desfosforilando os receptores AMPA e removendo este fósforo da membrana sináptica. Este processo também requer influxo de cálcio através do receptor NMDA.
A desativação do receptor NMDA por vários antagonistas induz vários problemas psiquiátricos em humanos, incluindo alucinação, transtorno do humor, delírio, pensamento anormal, agitação, falta de motivação, déficit cognitivo e outros problemas emocionais.
O bloqueio do receptor NMDA mediado por antagonistas (hipofuncionamento) leva à liberação excessiva de neurotransmissores excitatórios (glutamato e acetilcolina) em diferentes regiões do cérebro, o que, por sua vez, causa hiperestimulação de neurônios pós-sinápticos e subsequente indução de quadros psicóticos.
Os receptores NMDA sofrem um estado de hipofuncionamento com o avanço da idade. Esse hipofuncionamento se deve basicamente a uma redução dos sítios de ligação do ligante do receptor. Curiosamente, esse efeito é mais proeminente no córtex em comparação ao hipocampo.
Em pessoas com doenças neurodegenerativas relacionadas à idade, como a doença de Alzheimer, o grau de inativação do receptor NMDA é muito maior do que em pessoas saudáveis da mesma idade. Estudos propuseram que o hipofuncionamento do receptor NMDA pode induzir características neurodegenerativas semelhantes à doença de Alzheimer, e a amiloidose (deposição anormal de proteína beta-amilóide) pode deteriorar ainda mais o estado de hipofuncionamento do receptor NMDA. A contribuição coletiva desses processos pode eventualmente desencadear o início da doença de Alzheimer.
Aumentar o funcionamento do receptor NMDA por meio de várias drogas tornou-se uma estratégia terapêutica importante na prevenção da neurotoxicidade associada ao hipofuncionamento do receptor. Por exemplo, descobriu-se que drogas que aumentam a neurotransmissão GABAA reduzem a liberação excessiva de acetilcolina e subsequentemente previnem a neurotoxicidade causada pelo hipofuncionamento do receptor NMDA.
Da mesma forma, descobriu-se que drogas que ativam os receptores alfa-adrenérgicos reduzem a liberação de acetilcolina e previnem a neurotoxicidade e as complicações psiquiátricas causadas pelo hipofuncionamento do receptor NMDA.
Hiperativação do receptor NMDA
Tanto a hipofunção quanto a hiperativação do receptor NMDA são problemáticas (Zhou, & Sheng, 2013). O excesso de ativação é frequente em pacientes inflamados, com excesso de homocisteína e em casos de hipóxia. Também associa-se a doenças que cursam com excesso de glutamato, como Parkinson, Alzheimer, epilepsia, esclerose lateral amiotrófica, esquizofrenia, isquemia, transtorno do espectro autista. Leia sobre glutamato e neuroinflamação neste outro texto.
Como o receptor NMDA (NMSAR) pode ter papeis opostos?
Existem 2 modelos explicativos para o fenômeno. O modelo de localização (a) propõe que a ativação de NMDAR nas regiões extra-sinápticas (em marrom, na figura abaixo) leva à ativação de vias de sinalização de morte celular, enquanto a ativação de NMDARs sinápticos (em azul) é neuroprotetora.
O modelo de composição de subunidades (b) propõe que a ativação de GluN2B-NMDARs (verde) é excitotóxica, enquanto a ativação de GluN2A-NMDARs (laranja) é neurotrófica. Observe que os GluN2A-NMDARs são mais preferencialmente localizados na sinapse, enquanto os GluN2B-NMDARs são preferencialmente distribuídos nas regiões extra-sinápticas.
COMO MODULAR OS RECEPTORES NMDA?
Para modular os receptores NMDA é fundamental o combate à inflamação, ajuste de magnésio e zinco na dieta. Podemos também usar L-teanina e extrato de groselha negra para melhorar o funcionamento dos astrócitos e regular GABA, neurotransmissor que contrabalanceia o glutamato. Aprenda mais sobre nutrição e o cérebro em https://t21.video.
Melhorar a microbiota para reduzir a inflamação e prevenir doenças neurodegenerativas
Há evidências crescentes de estudos clínicos e pré-clínicos sugerindo que um desequilíbrio no microbioma intestinal (MI), conhecido como disbiose, desempenha um papel significativo no desenvolvimento de distúrbios neurodegenerativos, como a doença de Alzheimer (DA) e a doença de Parkinson (DP).
A pesquisa em andamento sobre o MI forneceu informações valiosas sobre a composição e as características do microbioma associado a doenças neurodegenerativas. Além disso, estudos demonstraram a influência de moléculas específicas derivadas do MI na neurodegeneração. Essas descobertas abriram novas possibilidades para o desenvolvimento de novos probióticos que poderiam tratar distúrbios neurodegenerativos de forma significativa.
Revisão publicada em 2023 resume o conhecimento atual sobre a composição e características do MI em relação às doenças neurodegenerativas.
Destaca-se a interação entre a suscetibilidade genética do hospedeiro à neurodegeneração e à disbiose intestinal. Corynebacterium, Porphyromonas e Prevotella interagem com as variantes genéticas rs356229, rs10029694 e rs6856813, respectivamente.
Além disso, Citrobacter rodentium interage com a neurotoxina microbiana ambiental BMAA , desencadeando disfunção mitocondrial e levando à neurodegeneração. Além disso, a autofagia defeituosa, a falha na eliminação de patógenos intracelulares induz alterações na composição do microbioma intestinal, num ciclo vicioso.
Também discute resultados de pesquisas sobre moléculas-chave derivadas do MI que afetam a neurodegeneração. Além disso, a revisão explora as aplicações potenciais de novos probióticos, incluindo Clostridium butyricum, Akkermansia muciniphila, Faecalibacterium prausnitzii e Bacteroides fragilis, no manejo e alívio de doenças neurodegenerativas.
Aprenda a modular a microbiota intestinal aqui.
Aprenda a interpretar testes nutrigenéticos aqui.