A metabolômica é uma abordagem analítica que estuda os metabólitos presentes em células, tecidos ou biofluidos. No contexto do câncer e da radioterapia, a metabolômica tem um papel crucial na compreensão dos efeitos da terapia, na identificação de biomarcadores e na personalização do tratamento.
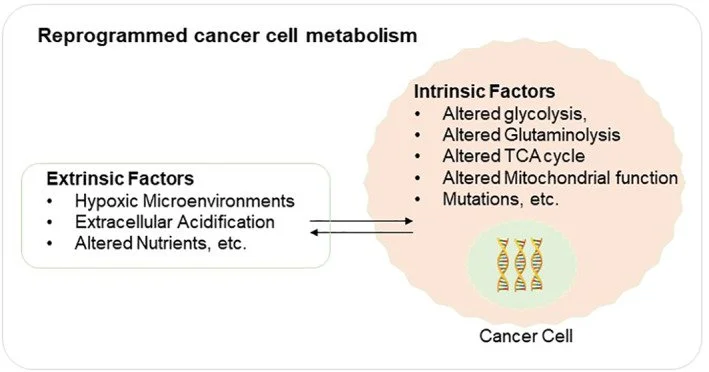
A metabolômica urinária reflete não apenas as alterações metabólicas internas das células tumorais, mas também as influências do microambiente tumoral. A figura abaixo mostra como o metabolismo das células é reprogramada por uma combinação de fatores intrínsecos (alterações na glicólise, glutaminólise, ciclo de Krebs, função mitocondrial, mutações) e fatores extrínsecos (hipóxia, acidez extracelular, disponibilidade de nutrientes).
Reprogramação metabólica em células cancerígenas (Suri et al., 2023)
Essa interação bidirecional gera perfis metabólicos característicos, que podem ser detectados em biofluidos como a urina. Assim, biomarcadores urinários relacionados a purinas, aminoácidos aromáticos, carnitinas e intermediários do ciclo de Krebs não apenas refletem a biologia tumoral intrínseca, mas também o impacto do microambiente, sendo valiosos para diagnóstico, monitoramento de resposta terapêutica e detecção de toxicidade.
1. Metabolômica no Tratamento do Câncer
A metabolômica permite identificar assinaturas metabólicas específicas de diferentes tipos de câncer e estados de progressão tumoral. Isso auxilia na:
Detecção precoce: Biomarcadores metabólicos podem indicar a presença de câncer antes que ele seja detectável por exames convencionais.
Caracterização do tumor: Tumores apresentam alterações metabólicas distintas, como o efeito Warburg (aumento do metabolismo glicolítico mesmo na presença de oxigênio).
Personalização da terapia: A resposta ao tratamento pode ser monitorada metabolicamente, permitindo ajustes na terapia.
2. Metabolômica na Radioterapia
A radioterapia atua induzindo danos ao DNA das células cancerígenas, mas também afeta células normais. A metabolômica pode ser aplicada para:
Monitorar resposta ao tratamento: Mudanças nos perfis metabólicos podem indicar a eficácia da radioterapia.
Identificar resistência: Algumas células tumorais desenvolvem resistência à radiação, muitas vezes alterando seu metabolismo. Fenilalanina, tirosina, triptofano e histidina são possíveis biomarcadores de progressão tumoral pós-tratamento.
Minimizar efeitos colaterais: Biomarcadores metabólicos podem prever toxicidade, ajudando a ajustar doses e proteger tecidos saudáveis.
3. Plataformas analísticas
Espectrometria de Massas (LC-MS/UPLC-MS): detecção de metabólitos polares e lipídicos (alta sensibilidade).
Ressonância Magnética Nuclear (NMR): menos sensível, mas muito reprodutível e quantitativo.
Cromatografia Líquida ou Gasosa acoplada à MS (LC-MS, GC-MS): ideal para ácidos orgânicos, aminoácidos, ácidos graxos voláteis.
Métodos usados na metabolômica (Suri et al., 2023)
4. Interpretação Biológica
A interpretação é feita mapeando os metabólitos em vias metabólicas (KEGG, HMDB, MetaboAnalyst).
Exemplos práticos:
a) Radiação e estresse oxidativo
↑ Hipoxantina, xantina, ácido úrico → ativação do metabolismo de purinas (turnover de DNA/RNA).
↑ Carnitinas (acetilcarnitina, TML, decanoylcarnitina) → alterações em transporte mitocondrial de ácidos graxos → sinalizam dano energético.
➡ Interpretação: indicadores precoces de dano por radiação e biodosimetria. Há necessidade de integração com outras bases (transcriptômica, proteômica) para fundamentar escolhas terapêuticas.
b) Progressão tumoral pós-radioterapia (câncer de mama)
Alterações em aminoácidos aromáticos (fenilalanina, tirosina, triptofano) → associados a inflamação crônica e biossíntese de neurotransmissores.
↓ Histidina → estresse oxidativo e resposta imune.
➡ Interpretação: podem prever resistência ou progressão da doença.
c) Diagnóstico de câncer de bexiga
Perfis alterados de piruvato, ácidos graxos, aminoácidos.
Alterações no metabolismo energético (efeito Warburg) → ↑ glicólise, ↓ ciclo de Krebs.
➡ Interpretação: assinatura metabólica tumoral detectável em urina com alta acurácia.
5. Integração com Clínica
Monitoramento: repetir coleta durante o tratamento → verificar se assinaturas metabólicas se aproximam de controles saudáveis ou de padrão de resposta.
Personalização: pacientes com perfis metabólicos de toxicidade (ex.: aumento de derivados de triptofano indicando inflamação intestinal) podem receber ajustes de dose/protetores.
Descoberta de alvos: se uma via (ex.: metabolismo de arginina/prolina) aparece alterada, pode sugerir terapias complementares (ex.: inibidores de arginase).
5. Desafios para o uso da metabolômica na oncologia
Há necessidade de maior padronização, estruturação de fluxos de pesquisa (coleta, extração de amostras, cromatografia, instrumentação, normalização, processamento e análises de dados multivariada). Boas práticas com controle de qualidade são fundamentais.
Fora isso, os custos dos testes ainda são elevados. Outro grande problema é a falta de expertise técnica para estudos na área.