A obesidade é uma doença complexa, que inclui em sua gênese fatores genéticos, hormonais, sociais, ambientais, econômicos. Hoje sabemos, por exemplo, que a regulação do nervo vago é importante para o controle da saciedade.
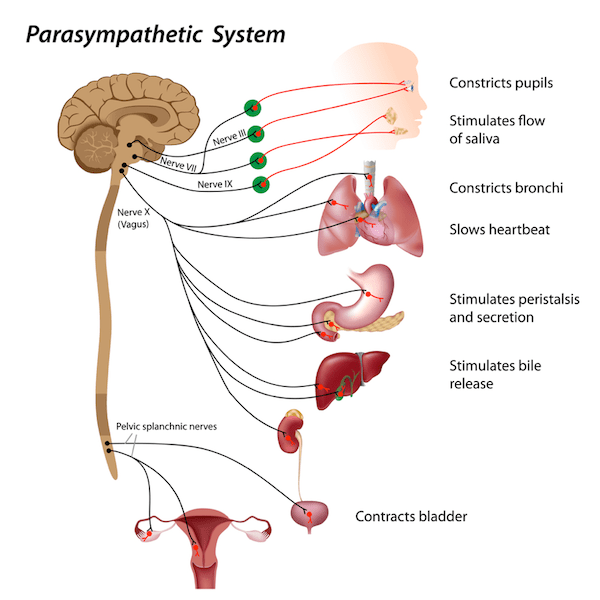
O termo “nervo vago” é, na verdade, a junção de milhares de fibras nervosas, organizados em 2 feixes que vão do tronco cerebral para baixo em cada lado do pescoço e no tronco, ramificando-se para tocar os órgãos internos, incluindo coração, intestino, pulmões, fígado, pâncreas, rins. Como capta muitos estímulos, o nervo vago – o mais longo dos 12 nervos cranianos – às vezes é chamado de “superestrada da informação”.
Estudos indicam que estimular o nervo vago pode ajudar pessoas com epilepsia, diabetes, depressão resistente ao tratamento medicamentoso, transtorno de estresse pós-traumático, transtorno de ansiedade, condições autoimunes inflamatórias, como doença de Crohn ou artrite reumatoide e também no controle da compulsão alimentar.
O eixo intestino-cérebro
É formado pelo sistema nervoso central (SNC), a inervação entérica que inclui fibras extrínsecas do sistema nervoso autônomo (SNA) e neurônios intrínsecos do sistema nervoso entérico (SNE), o eixo hipotálamo-hipófise-adrenal (HPA) e a microbiota intestinal.
A funcionalidade do trato GI (motilidade intestinal, função secretora, fluxos de fluidos ou fluxo sanguíneo) é regulada pela ação integrada do SNC e do SNE. Enquanto o SNC controla as funções intestinais por meio das inervações extrínsecas do SNA, o SNE pode agir de forma autônoma e independente do cérebro.
O SNE é composto por milhões de neurônios. As inervações entéricas são separadas do conteúdo luminal intestinal, incluindo a microbiota, pela barreira celular epitelial, pela camada mucosa e pelas secreções iônicas e líquidas. No entanto, a microbiota intestinal se comunica com as inervações entéricas por meio de vários possíveis rotas que podem envolver interações intermediárias com células imunes e células enteroendócrinas (EECs).
As EECs produzem hormônios intestinais (por exemplo, colecistoquinina (CCK) ou peptídeo semelhante ao glucagon 1 (GLP-1) em resposta a estímulos bacterianos, que também modulam a atividade de inervação entérica; por sua vez, neurônios entéricos fazem sinapse em EECs permitindo alimentação mútua de volta. Portanto, a microbiota poderia influenciar o ENS por meio de sua interação direta com o funcionamento do EEC.
Muitos dos sinais de saciedade são hormônios anorexígenos, como peptídeo YY (PYY), GLP-1, neuropeptídeo inibidor gástrico (GIP), CCK, oxintomodulina (OXM) e prouroguanilina (Pimentel et al., 2012). Esses sinais são ativados durante o período pós-prandial. No entanto, durante o período de jejum, hormônios orexígenos como a grelina são liberados principalmente no estômago e excretados para a circulação periférica. Além disso, diferentes neuropeptídeos como a proteína relacionada agouti (AgRP) e o neuropeptídeo Y (NPY) são ativados em neurônios hipotalâmicos durante o jejum para produzir uma sensação de fome e uma resposta comportamental: ou seja, para começar a comer.
Mudanças na alimentação em resposta ao controle do apetite do SNC podem influenciar a disponibilidade de nutrientes para a microbiota intestinal e, posteriormente, sua composição. Por sua vez, a modulação da microbiota intestinal e sua atividade por intervenção dietética também podem modificar os sinais de saciedade. Quando as bactérias intestinais metabolizam prebióticos como oligofrutose (OFS) ou inulina, elas produzem ácidos graxos de cadeia curta que podem aumentar a expressão gênica de GLP-1 e PYY no trato intestinal induzindo a saciedade.
Algumas cepas probióticas pertencentes aos gêneros Bifidobacterium e Lactobacillus também influenciam o nervo vago e, como consequênica, há melhoria no humor e redução da ansiedade. Outro mecanismo pelos quais os probióticos podem mediar esses efeitos incluem suas possíveis propriedades reguladoras do sistema imunológico e a pordução de serotonina (5-HT). O 5-HT é um neurotransmissor monoamínico produzido a partir do triptofano, ingerido na dieta. Este neurotransmissor é bem conhecido por seu papel na cognição e humor no cérebro. Aproximadamente 95% da 5-HT é produzida no intestino.
As funções clássicas atribuídas ao 5-HT no trato GI estão relacionadas à sua participação na motilidade GI, secreção e percepção da dor. A 5-HT também tem ações de fator trófico neuroprotetor e ações pró-inflamatórias no intestino.
Técnicas para estimular o nervo vago
1) SOM
- Encontre um local calmo
- Coloque sua música ou mantra favorito (KALYANI, et al, 2011).
- Feche os olhos
- Cante junto
2) YOGA
A respiração lenta, a entoação de mantras como o OM, as posturas (ásanas) e as técnicas de concentração ajudam a ativar o nervo vago (STREETER et al. 2010).