A inflamação é uma resposta natural do corpo a lesões ou infecções. Ela é essencial para a defesa e reparo dos tecidos, mas, quando descontrolada, pode se tornar prejudicial, contribuindo para o desenvolvimento de doenças crônicas. O processo de resolução da inflamação é ativo e regulado, permitindo que o corpo encerre a inflamação de forma eficiente e restaure a homeostase tecidual.
O que é Inflamação?
O termo inflamação, ou flogose, deriva do latim inflamare e do grego flogós, que significa “pegar fogo”. Trata-se de uma resposta do sistema imunológico em tecidos vascularizados, caracterizada pela saída de células e moléculas do sangue para o tecido afetado.
Essa resposta é desencadeada por um agente inflamatório (flogógeno), que estimula a liberação de mediadores pró-inflamatórios. Esses mediadores aumentam a permeabilidade dos vasos sanguíneos e favorecem a exsudação, permitindo que células de defesa, como os neutrófilos, cheguem ao local da lesão ou infecção.
O organismo busca sempre um equilíbrio entre mediadores pró-inflamatórios e anti-inflamatórios. Quando esse equilíbrio é perdido, podem surgir processos patológicos.
Sinais Clássicos da Inflamação
Os sinais cardinais da inflamação foram inicialmente descritos por Celsus e incluem:
Calor
Rubor (vermelhidão)
Tumor (inchaço/edema)
Dor
Posteriormente, Virchow acrescentou a perda ou redução da função da área afetada.
A Cascata Inflamatória
Quando ocorre uma lesão celular, fosfolipídios da membrana são expostos, iniciando a cascata inflamatória, também conhecida como cascata do ácido araquidônico.
Essa cascata leva à produção de mediadores inflamatórios, como leucotrienos e prostaglandinas, por meio de enzimas como:
Lipoxigenases
Ciclooxigenases (COX-1 e COX-2)
Em especial, a COX-2 é responsável por estimular e perpetuar a inflamação.
Mediadores Lipídicos: Os Arquitetos da Resolução
Durante a inflamação, o corpo produz mediadores lipídicos pró-resolução, derivados de ácidos graxos essenciais como o ácido araquidônico e o ácido eicosapentaenoico.
Entre eles, destacam-se:
Lipoxinas
Resolvinas
Maresinas
Protectinas
Esses mediadores atuam de forma coordenada para resolver a inflamação sem comprometer a resposta imunológica necessária, promovendo a restauração do equilíbrio nos tecidos.
Papel das lipoxinas, resolvinas e maresinas
Lipoxinas: Inibem a migração excessiva de neutrófilos, promovem sua apoptose (morte celular programada) e estimulam os macrófagos a fagocitar células mortas, facilitando a limpeza do local inflamatório.
Resolvinas: Derivadas do ácido eicosapentaenoico (EPA), as resolvinas promovem a resolução da inflamação e a regeneração tecidual. Por exemplo, a RvD2 induz a resolução ativa da inflamação e a regeneração tecidual em lesões periapicais, enquanto a RvD1 controla o microambiente inflamatório em defeitos em calvárias, promovendo a cicatrização óssea e a angiogênese.
Maresinas: Derivadas do ácido docosahexaenoico (DHA), as maresinas, como a MaR1, induzem a proliferação e migração de células-tronco mesenquimais, osteogênese e angiogênese em defeitos em calvárias, promovendo a regeneração óssea em defeitos craniofaciais e alveolares.
A falha na resolução da inflamação pode levar a condições como artrite reumatoide, doença inflamatória intestinal e aterosclerose. Compreender e manipular esses mediadores oferece novas perspectivas terapêuticas para tratar essas doenças.
❌ E quando a inflamação não se resolve?
A inflamação falha em se resolver quando o equilíbrio entre sinais pró-inflamatórios e pró-resolução é perturbado. Algumas causas comuns incluem:
Produção insuficiente de mediadores pró-resolução (SPMs)
O corpo não consegue gerar lipoxinas, resolvinas, maresinas ou protectinas suficientes.
Ex.: em doenças crônicas como artrite reumatoide ou doença inflamatória intestinal, há deficiência de SPMs locais.
Excesso de sinais pró-inflamatórios
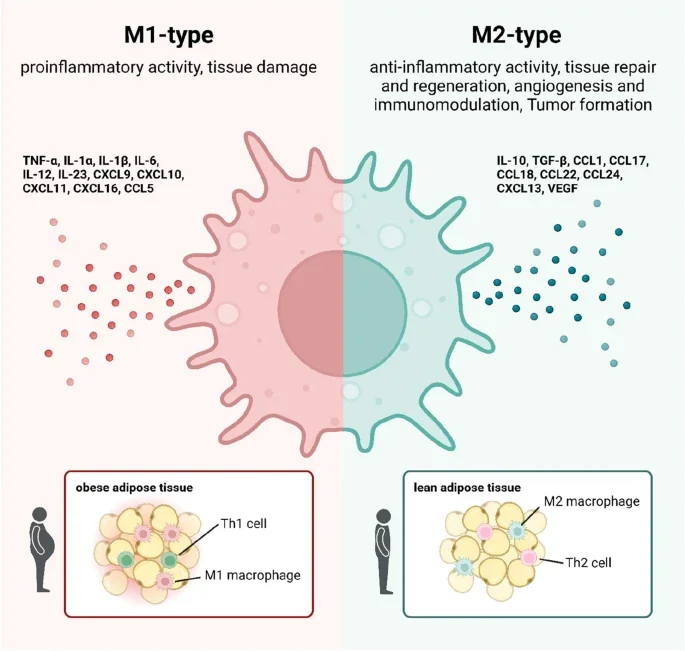
Citocinas como TNF-α, IL-1β e IL-6 continuam ativas por muito tempo, mantendo neutrófilos e outros leucócitos no tecido.
Falha na fagocitose de células mortas
Macrófagos não conseguem “limpar” neutrófilos apoptóticos ou restos celulares. Isso prolonga o estado inflamatório e pode induzir dano tecidual.
Alterações metabólicas e oxidativas
Estresse oxidativo, obesidade ou diabetes podem interferir na produção e ação dos SPMs.
Infecção persistente ou estímulo contínuo
Exposição constante a patógenos ou irritantes mantém a inflamação ativa.
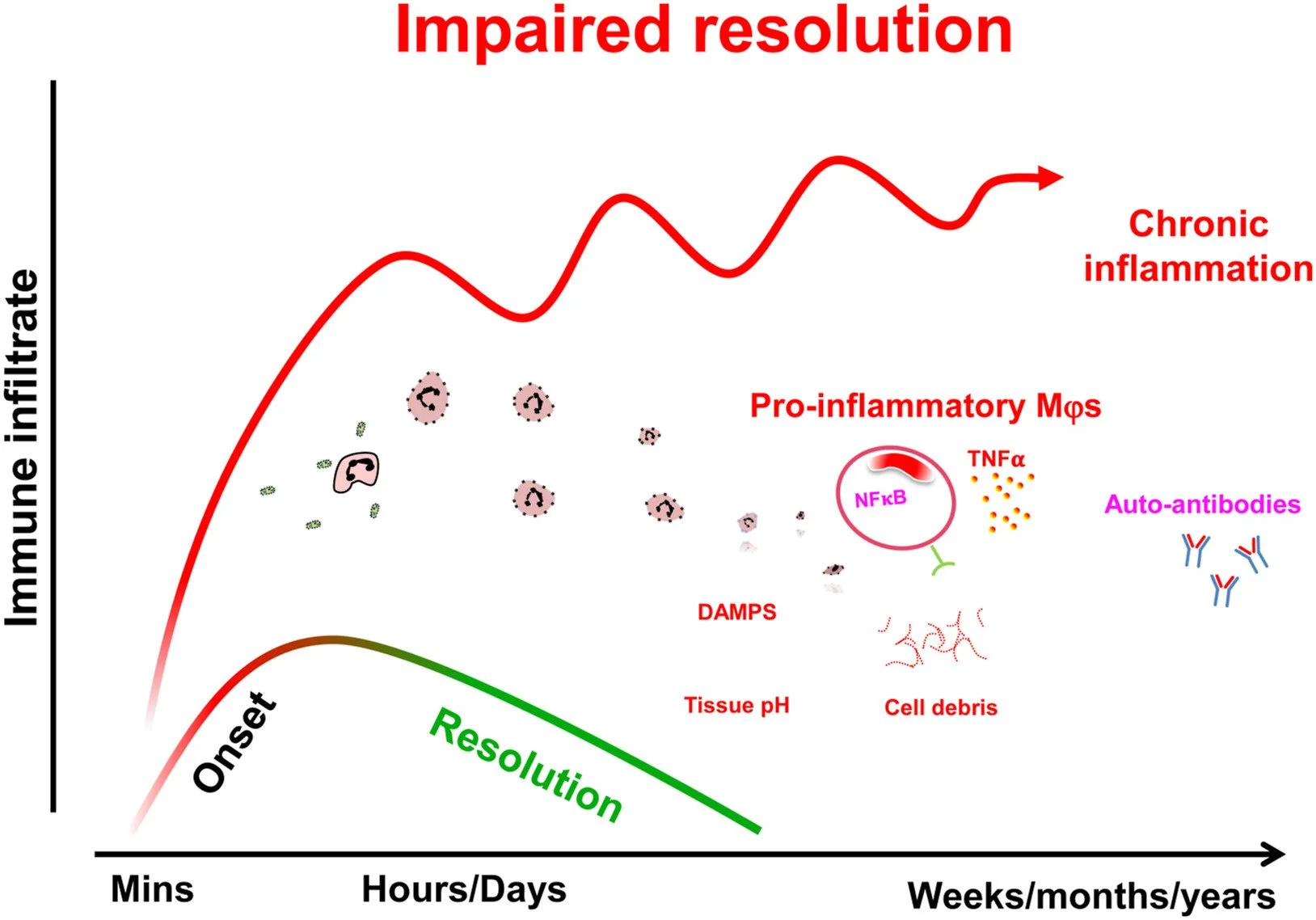
O que é inflamação crônica?
Inflamação crônica ocorre quando o processo inflamatório não se resolve adequadamente. Em vez de desaparecer, ele persiste semanas, meses ou até anos, causando danos progressivos aos tecidos.
Já vimos causas comuns: infecções persistentes, exposição contínua a toxinas, obesidade, estresse oxidativo, doenças autoimunes ou falha na produção de mediadores pró-resolução (SPMs).
Consequências da inflamação crônica
Dano tecidual progressivo
Neutrófilos e macrófagos liberam enzimas e radicais livres. Isso destrói estruturas celulares e matrizes extracelulares.
Ex.: na artrite reumatoide, destruição da cartilagem e do osso.
Fibrose e cicatrização desordenada
O tecido tenta se regenerar, mas com excesso de colágeno e matriz extracelular. Resulta em tecido cicatricial rígido que compromete função.
Ex.: fibrose hepática em hepatite crônica.
Alterações funcionais dos órgãos
Inflamação crônica altera a função normal.
Ex.: em doença inflamatória intestinal, absorção intestinal prejudicada; em aterosclerose, vasos rígidos e estreitos.
Desregulação imunológica
Ativação contínua do sistema imune pode levar a autoimunidade.
Ex.: lúpus eritematoso sistêmico ou esclerose múltipla.
Risco aumentado de câncer
Inflamação persistente gera mutações e alterações no microambiente tecidual.
Ex.: gastrite crônica por H. pylori aumenta risco de câncer gástrico.
Metabolismo alterado
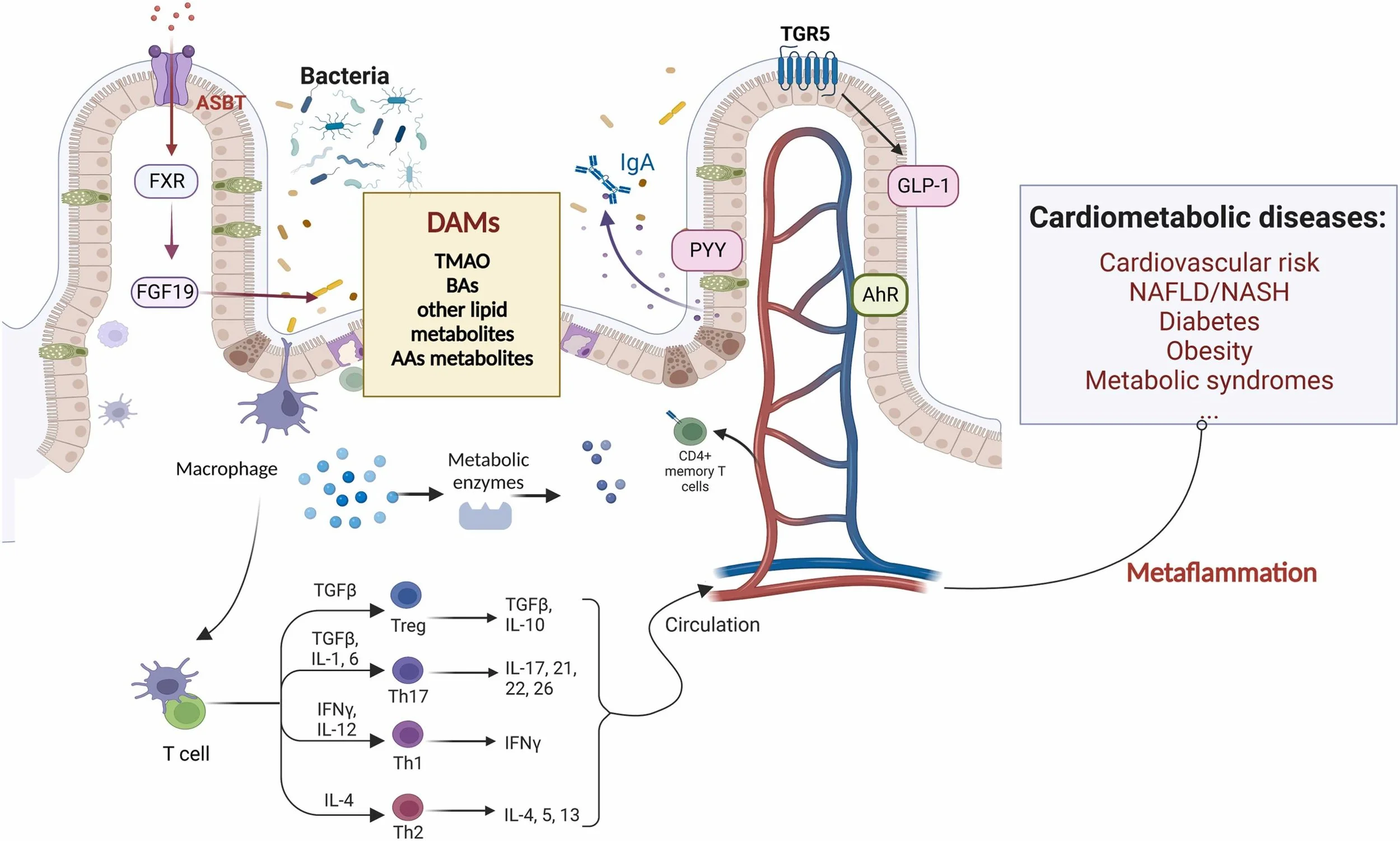
Inflamação crônica está associada a resistência à insulina, obesidade e doenças cardiovasculares.
Ex.: citocinas inflamatórias interferem na sinalização da insulina e no metabolismo lipídico.
Como reduzir a inflamação crônica
Pode existir necessidade de uso de medicação antiinflamatória que bloqueia citocinas ou enzimas que perpetuam a inflamação (como COX-2 em certos contextos) cria um ambiente favorável à ação dos SPMs.
Uso de precursores de mediadores lipídicos importantes:
Ácidos graxos ômega-3 (EPA e DHA) são substratos para a síntese de resolvinas e maresinas.
Dietas ricas em ômega-3 aumentam a produção natural desses mediadores.