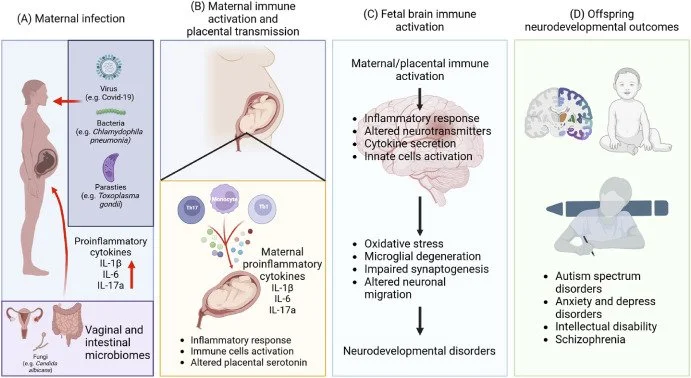
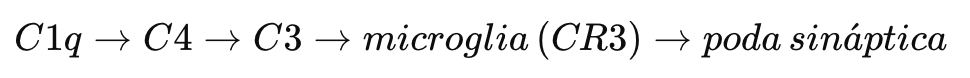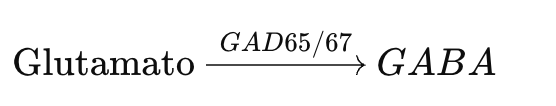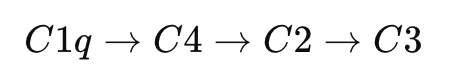Infecção materna, obesidade, autoimunidade, disbiose ou inflamação sistêmica durante a gestação induzem “maternal immune activation” (MIA). Isso aumenta IL1b, IL-6, IL-17A, TNF-α e ativa microglia fetal (Han et al., 2021, Yin et al., 2024; Croen et al., 2023; Gardner et al., 2025).
A microglia ativada passa a expressar mais proteínas do complemento, especialmente C1q e C3. O sistema complemento, tradicionalmente associado à imunidade inata, também atua no cérebro regulando poda sináptica, plasticidade e homeostase neuronal. O cérebro em desenvolvimento usa esse sistema fisiologicamente para selecionar quais sinapses devem permanecer e quais serão eliminadas (Stevens, & Johnson, 2021) Marca sinapses fracas ou desnecessárias para eliminação por micróglias. Esse processo é fisiológico e essencial para a maturação dos circuitos neurais.
O C1q liberado favorece ativação da micróglia e pode aumentar a inflamação via NF-kB, elevando expressão de pro-IL e NLRP3. Isso desloca o metabolismo neural e glial para um estado glicolítico inflamatório, com aumento de lactato, disfunção mitocondrial e redução da eficiência oxidativa. O resultado é um eixo pro-apoptótico mediado pela neuroinflamação sustentada.
C1q “marca” sinapses imaturas ou pouco ativas.
C3b/iC3b opsoniza essas sinapses.
A microglia reconhece via CR3 e fagocita.
Isso é essencial para o neurodesenvolvimento normal. O problema surge quando há hiperativação crônica ou timing inadequado. Em modelos animais, excesso de C1q/C3 está associado a poda excessiva, perda sináptica excessiva e alteração de circuitos corticais (Gomez-Arboledas, Acharya, & Tenner, 2021).
A ativação aberrante do complemento está associada a múltiplas doenças neurodegenerativas e neuroinflamatórias:
Alzheimer
Esclerose múltipla
Traumatismo craniano
AVC
Infecção por Zika
Lesão por radioterapia cerebral
Os interneurônios GABAérgicos parecem particularmente vulneráveis porque amadurecem tardiamente e dependem muito de refinamento sináptico adequado. Modelos de ativação imune materna mostram (Gillespie et al., 2023):
• redução de parvalbumina, proteína ligadora de cálcio, altamente expressa em alguns interneurônios GABAérgicos rápidos do córtex e hipocampo. O resultado é a pior integração temporal de informação sensorial e cognitiva.
• alteração de GAD65/GAD67, enzimas de síntese de GABA a partir de glutamato.
GAD65 (GAD2): associado a terminais sinápticos e liberação rápida
GAD67 (GAD1): manutenção basal de GABA intracelular
Redução funcional de GAD implica em menor disponibilidade de GABA sináptico, redução de inibição tônica e fásica, maior excitabilidade de redes piramidais.
• defeito em interneurônios corticais, leva a redução de arborização dendrítica, falha de migração ou posicionamento cortical, redução da conectividade inibitória local.
• desequilíbrio excitação/inibição. Quando E/I aumenta há maior excitabilidade cortical, menor limiar de ativação sensorial, com vários efeitos sistêmicos possíveis:
déficit de atenção e menor controle inibitório
impulsividade
hipersensibilidade sensorial
labilidade emocional
maior carga de esforço cognitivo
pior consolidação de memória de trabalho
maior vulnerabilidade a estresse e privação de sono
Assim, a inflamação materna leva a uma microglia hiperreativa, com complemento aumentado, poda aberrante e circuitos GABAérgicos disfuncionais.
Sobre C4
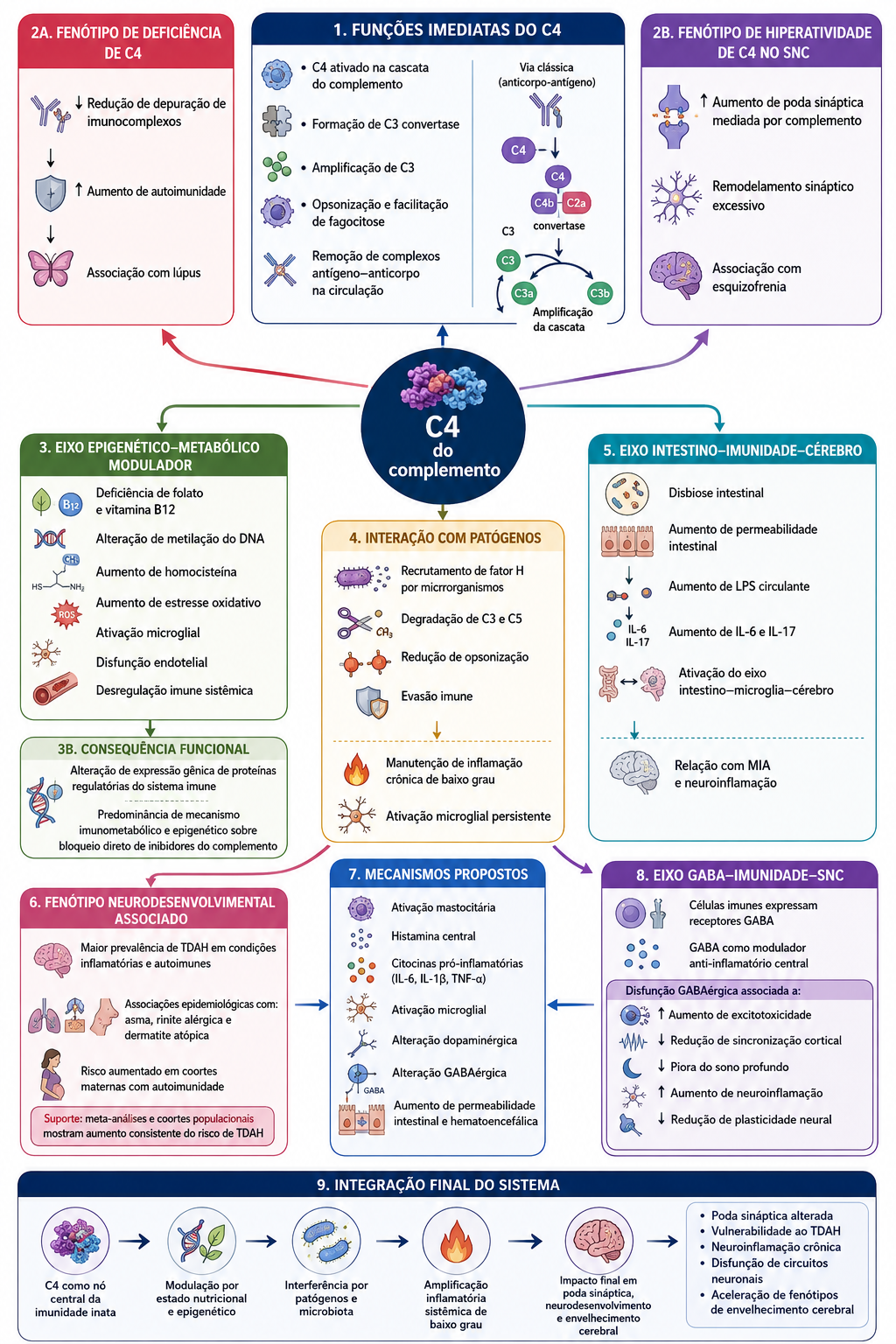
C4 refere-se ao componente 4 do sistema complemento.
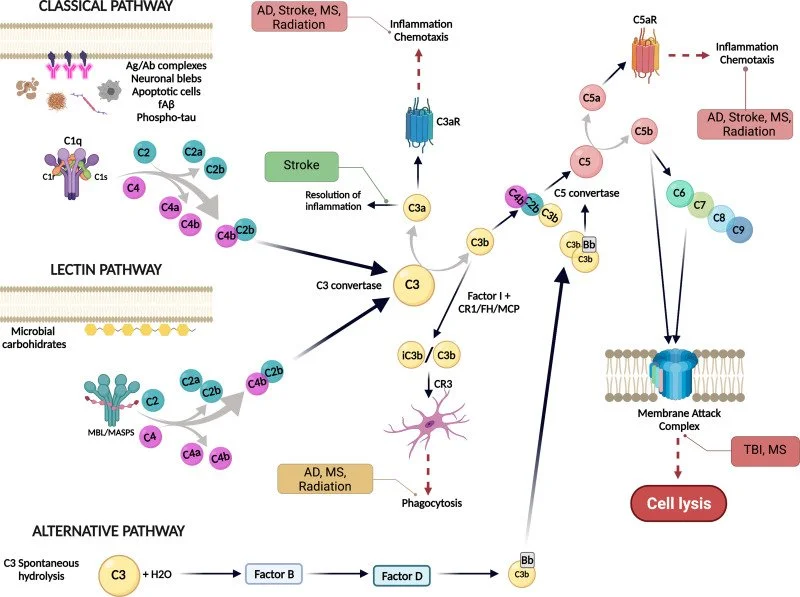
Via clássica do complemento
C4 liga-se a superfícies e facilita reconhecimento por fagócitos, forma o complexo C3, amplificando a cascata, participa da remoção de complexos antígeno-anticorpo na circulação.
A deficiência de C4 aumenta a autoimunidade, como no lúpus, leva a falha da depuração de imunocomplexos. Já o aumento da atividade de C4, especialmente no cérebro, está associado a aumento da poda sináptica, com implicações na esquizofrenia (Hogenaar, Bokhoven, 2021).
Os cuidados maternos para redução da inflamação são fundamentais na gestação. Além disso, o tratamento de carências nutricionais é imprescindível, uma vez que:
• deficiência de folato/B12 → metilação alterada
• aumento de homocisteína
• estresse oxidativo
• ativação microglial
• disfunção endotelial
• pior regulação imune
A deficiência de metilação também altera expressão gênica de proteínas regulatórias imunes. Portanto, o vínculo é mais epigenético/imunometabólico do que um bloqueio direto de “inibidores do complemento”.
Patógenos conseguem modular complemento e escapar da imunidade. Vários microrganismos:
• recrutam fator H
• degradam C3/C5
• reduzem opsonização
• alteram regulação imune
Isso pode perpetuar inflamação crônica de baixo grau e ativação microglial persistente.
Além disso, disbiose intestinal altera:
• permeabilidade intestinal
• LPS circulante
• IL-6/IL-17
• eixo microglia-intestino
e isso conversa diretamente com MIA e neuroinflamação (Han et al., 2021). Nos trantornos do desenvolvimento a imunidade pode estar alterado. Há suporte epidemiológico consistente para associação entre TDAH e doenças atópicas, inflamatórias e autoimunes. Não é causalidade única, mas correlação replicada em coortes grandes, meta-análises e estudos de registro.
Meta-análises e coortes populacionais mostram aumento de risco de TDAH em crianças com doenças atópicas.
Achados típicos:
• maior prevalência de TDAH em asma e rinite alérgica
• associação com dermatite atópica (eczema)
• relação dose-resposta em algumas coortes (mais doenças atópicas → maior risco de sintomas atencionais)
Estudos-chave:
• Miyazaki et al. (2017), meta-análise: associação entre asma e TDAH
• Schmitt et al. (2013), dermatite atópica e TDAH em coortes pediátricas
• Nielsen et al. (2021), JAMA Psychiatry: doenças autoimunes maternas aumentam risco de TDAH
• Walle et al. (2025), BMC Med: doenças autoimunes e inflamatórias maternas são associadas a maior risco de TDAH nos filhos
Os mecanismos propostos incluem:
• ativação mastocitária
• histamina cerebral
• citocinas pró-inflamatórias
• microglia ativada
• alteração dopaminérgica
• alteração GABAérgica
• permeabilidade intestinal (Aarts et al., 2017) e hematoencefálica (Sayed et al., 2024)
A microglia cronicamente ativada pode manter circuitos em estado “imaturo”. Isso ajuda a explicar hipersensibilidade sensorial, fadiga cognitiva, disfunção autonômica e maior vulnerabilidade ao estresse inflamatório.
Células do sistema imune possuem receptores GABA para conter a inflamação no sistema nervoso central (Tian, & Kaufman, 2023). A disfunção GABAérgica crônica associa-se a:
• maior excitotoxicidade
• menor sincronização cortical
• pior sono profundo
• aumento de neuroinflamação
• redução de plasticidade
Este artigo propõe que disfunção GABAérgica é um mecanismo central que liga envelhecimento, hiperatividade de redes neurais e declínio de memória episódica na doença de Alzheimer. Ou seja, a disfunção pode acelerar fenótipos de envelhecimento cerebral. Mais nos cursos de saúde de precisão.