Cetonas são substâncias produzidas pelo fígado durante as dietas com baixo teor de carboidratos. Possuem múltiplos efeitos metabólicos e moleculares que favorecem a manutenção e restauração da homeostase cerebral, especialmente em contextos de estresse metabólico e neurodegeneração. A fisiologia subjacente envolve metabolismo energético, regulação de estresse oxidativo, sinalização celular e mecanismos de proteostase.
Mecanismos principais
1) Substituição de combustível e otimização metabólica
As cetonas (principalmente β-hidroxibutirato e acetoacetato) entram no cérebro através de transportadores monocarboxilatos (MCTs) e são oxidadas nas mitocôndrias, gerando acetil-CoA para o ciclo de Krebs e fosforilação oxidativa. Isso fornece ATP de forma eficiente quando a glicose está limitada ou hipometabólica.
A utilização de cetonas diminui a necessidade de glicólise e pode reduzir a produção de espécies reativas de oxigénio (ROS) porque a fosforilação oxidativa de cetonas é mais eficiente em termos de relação ATP/oxigénio do que o metabolismo da glicose.
2) Redução do estresse oxidativo e inflamação
Cetonas modulam vias celulares que reduzem ROS e sinais pró-inflamatórios, incluindo ativação de fatores antioxidantes e inibição de inflamassomas como o NLRP3.
Elas também influenciam a expressão de genes antioxidantes por meio de sinalização epigenética (por exemplo, modulação de HDAC ou sirtuínas), aumentando a resistência ao estresse oxidativo.
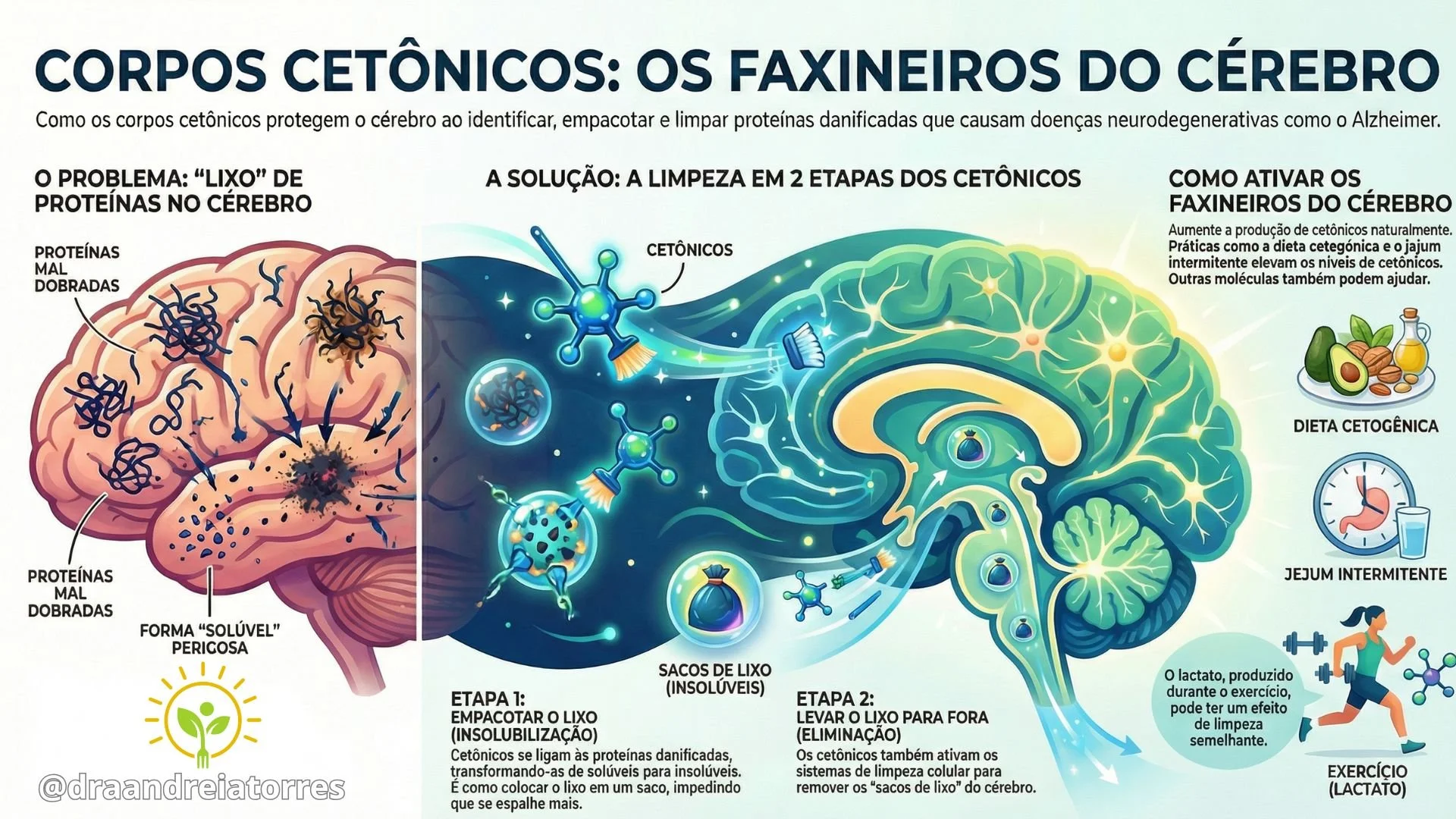
3) Modulação de autofagia e “limpeza” de proteínas danificadas
Há evidência emergente de que β-hidroxibutirato facilita a autofagia e a biogênese lisossomal, mecanismos celulares de degradação e reciclagem de proteínas e organelos disfuncionais, crucial para remover agregados proteicos e detritos celulares.
Estudos pré-clínicos (evidência recente) mostram que cetonas podem alterar a solubilidade de proteínas mal dobradas, facilitando sua eliminação por vias de autofagia/lysossomal, reduzindo agregados associados a neurodegeneração.
4) Regulação de vias de sobrevivência celular e sinalização
Cetonas ativam sensores metabólicos como SIRT1/AMPK/PGC-1α, promovendo biogênese mitocondrial e melhorando a capacidade oxidativa das mitocôndrias.
Elas também influenciam neurotransmissão e equilíbrio excitador/inibitório (ex: GABA/glutamato), o que pode limitar excitotoxicidade neuronal.
5) Redução de neuroinflamação e suporte glial
Ao suprimir ativação microglial pró-inflamatória e promover fenótipos anti-inflamatórios, cetonas ajudam a reduzir sinais inflamatórios crónicos que contribuem para disfunção neuronal.
Resumindo, as cetonas melhoram a eficiência energética mitocondrial, reduzem estresse oxidativo, ativam vias de detoxificação e autofagia, e modulam respostas inflamatórias e epigenéticas. Esses efeitos combinados promovem a manutenção e remoção de componentes intracelulares danificados e proteicos através de mecanismos celulares de qualidade proteica e metabolismo energético favorável, o que tem sido interpretado como um “efeito de limpeza” neuroprotectivo em contextos patológicos.
A plataforma da saúde metabólica: https://t21.video