Qualquer ativação do sistema imune inato ou adaptativo fora do Sistema Nervoso Central (SNC) é chamada de inflamação periférica. Contudo, uma infecção periférica inicial pode perturbar a função do SNC, com respostas que vão desde pequenas perturbações na temperatura corporal até fadiga severa e perda de consciência.
A inflamação aguda de curto prazo normalmente não afeta a homeostase do cérebro, graças à defesa proporcionada por uma barreira hematoencefálica intacta. No entanto, a inflamação periférica grave pode envolver o SNC e desencadear a neuroinflamação, por cinco mecanismos distintos:
1) As citocinas circulantes podem chegar ao cérebro pelo sistema glinfático:
2) Certas citocinas podem ser transportadas através da barreira hematoencefálica, embora esse processo provavelmente varie entre regiões do cérebro e condições fisiológicas, e entre diferentes citocinas.
3) As citocinas e quimiocinas são conhecidas por se comunicarem e ativarem os órgãos circunventriculares, o que permite a entrada de moléculas de baixo peso molecular quando há aumento da permeabilidade da barreira hematoencefálica.
4) O quarto ponto de entrada conhecido é através da ativação dos nervos periféricos via citocinas.
5) O plexo coróide, com seus capilares fenestrados, também pode ser um ponto de entrada para patógenos estranhos e células imunes em circulação. O plexo coróide é essencial para a homeostase do fluido cerebral e estudos recentes mostram que ele pode se comunicar com células gliais residentes no parênquima cerebral adjacente por meio de vesículas extracelulares.
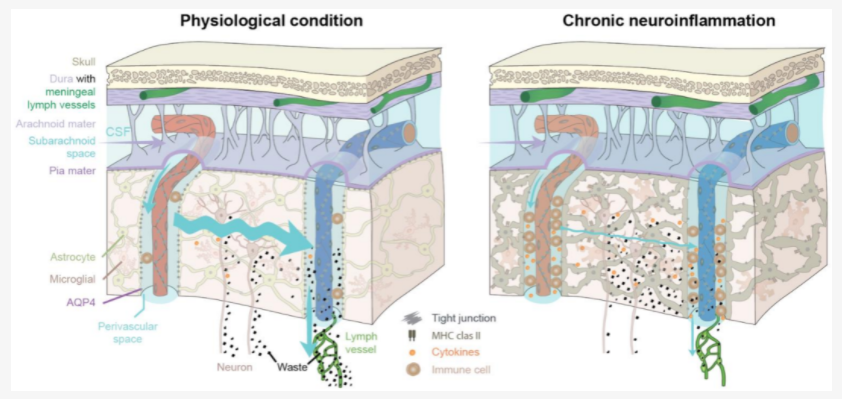
Sistema glifático e neuroinflamação
Uma das importantes causas de inflamação periférica é a disbiose intestinal. Quando bactérias ruins morrem liberam lipopolissacarídeos bacterianos (LPS) que chegam à circulação e entram no cérebro. Quando o sistema glifático reage bem, remove estas toxinas. Mas quando não funciona adequadamente o acúmulo de LPS e outras substâncias gera neuroinflamação (figura abaixo à direita).
Consequências da neuroinflamação
O acúmulo de resíduos e citocinas irá conduzir ainda mais a inflamação, em um ciclo vicioso. O inchaço cerebral resultante gera dores de cabeça, enxaqueca, afeta o comportamento, interfere no sono, memória e cognição. Pode contribuir para o dano neuronal e aumentar o risco de processos neurodegenerativos, como a doença de Alzheimer.
Embora os transtornos psiquiátricos tenham sido tradicionalmente explicados por alterações em neurotransmissores e conectividade neural, evidências recentes sugerem que a disfunção glinfática desempenha um papel crucial em sua patofisiologia.
A disfunção do sistema glinfático impacta a saúde mental por meio de três caminhos principais:
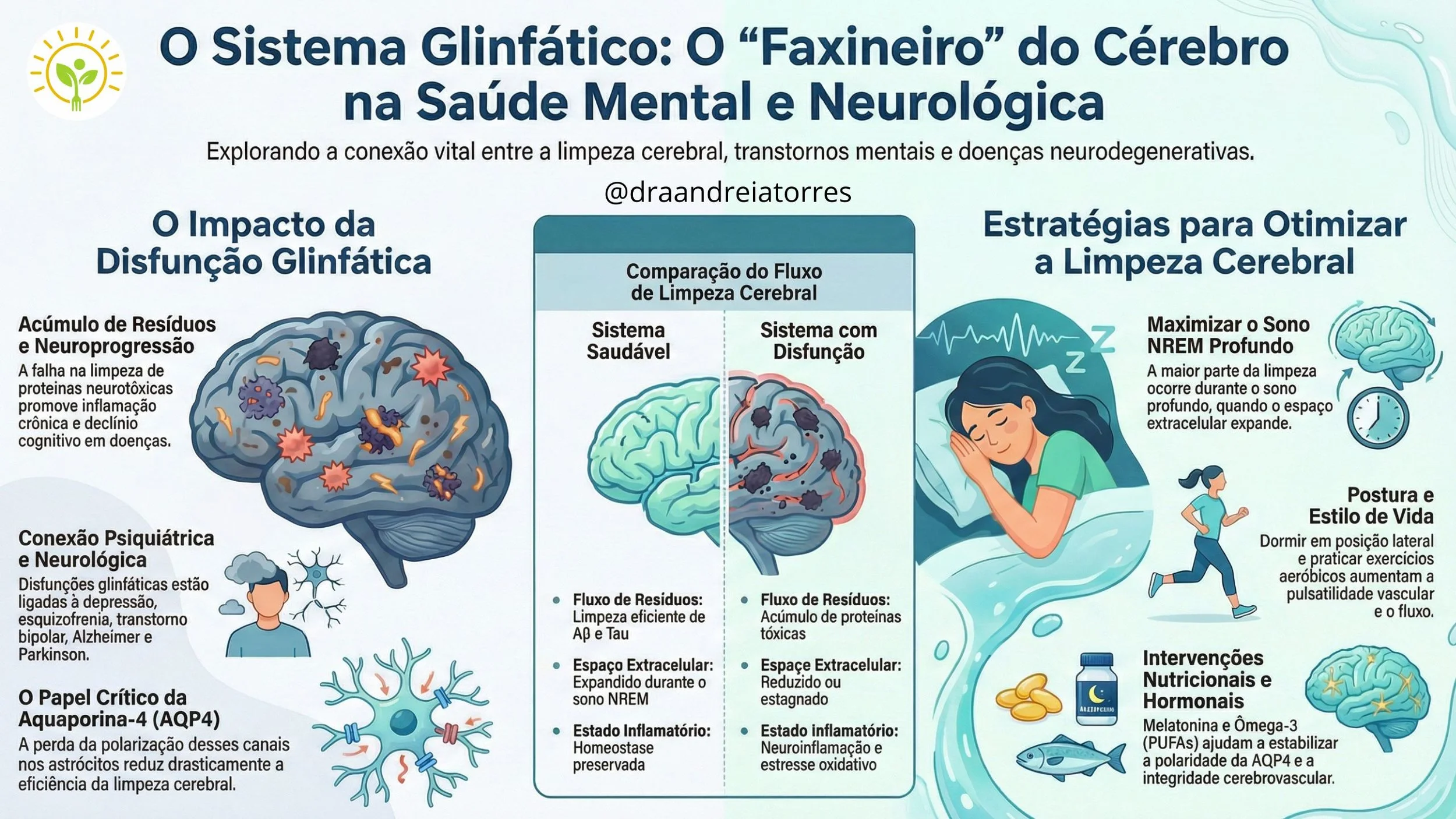
• Via de limpeza direta: Quando o fluxo perivascular diminui, a remoção de proteínas neurotóxicas (como beta-amiloide e tau), espécies reativas de oxigênio e citocinas é prejudicada, promovendo neuroinflamação e sinaptopatia.
• Via mediada pelo sono e ritmo circadiano: O sistema glinfático é mais ativo durante <o sono profundo (não-REM). A insônia e a fragmentação do sono, comuns em transtornos psiquiátricos, reduzem a capacidade de limpeza, criando um ciclo vicioso de inflamação e sintomas persistentes.
• Via vascular-metabólica-imune: O endurecimento arterial e a inflamação sistêmica degradam a pulsatilidade que impulsiona o fluido glinfático, aumentando a resistência hidráulica e sustentando a neuroinflamação crônica.
Evidências em Transtornos Específicos
Estudos de neuroimagem, utilizando principalmente o índice DTI-ALPS (que mede a difusão ao longo dos espaços perivasculares), encontraram alterações em diversas condições:
• Depressão (TMD): Pacientes apresentam redução no índice ALPS, o que se correlaciona com fadiga, sintomas cognitivos e marcadores inflamatórios sistêmicos.
• Esquizofrenia e Psicose: Alterações na limpeza glinfática já são visíveis em estágios iniciais da psicose e em pacientes que nunca usaram antipsicóticos, sugerindo que o déficit é intrínseco à doença e ligado a sintomas negativos e cognitivos.
• Transtorno Bipolar: Ciclos irregulares de sono-vigília e estresse metabólico convergem para a ineficiência glinfática, com evidências de mudanças no fluido extracelular e atrofia no polo frontal associada a essa disfunção.
• Transtorno de Estresse Pós-Traumático (TEPT): O estado de hiperalerta e o tom noradrenérgico elevado suprimem a vasomoção lenta, essencial para o fluxo glinfático, o que pode perpetuar memórias de medo e fragmentação do sono.
• Transtornos do Neurodesenvolvimento (TDAH e TEA): Disfunções glinfáticas foram observadas tanto em crianças quanto em adultos, sugerindo que falhas na troca de fluidos podem influenciar trajetórias de atenção, execução e comunicação social.
Implicações Terapêuticas e Farmacológicas
• Otimização do sono: Priorizar intervenções que aprofundem o sono NREM para expandir os espaços extracelulares e facilitar a limpeza.
• Cronofarmacoterapia: Alinhar a administração de medicamentos com os picos de fluxo glinfático para melhorar a eficácia e reduzir efeitos colaterais causados pelo acúmulo desigual de drogas.
• Suporte aos astrócitos e vasos: O uso de melatonina, ácidos graxos ômega-3 e exercícios aeróbicos pode proteger a integridade cerebrovascular e a polarização da AQP4.
• Agentes específicos: Medicamentos como a dexmedetomidina são considerados "amigáveis ao sistema glinfático", enquanto o uso crônico de benzodiazepínicos e o consumo de álcool podem degradar a arquitetura do sono e o transporte de fluidos (Wang et al., 2025).
No vídeo abaixo você conhecerá algumas formas de cuidar do seu cérebro.