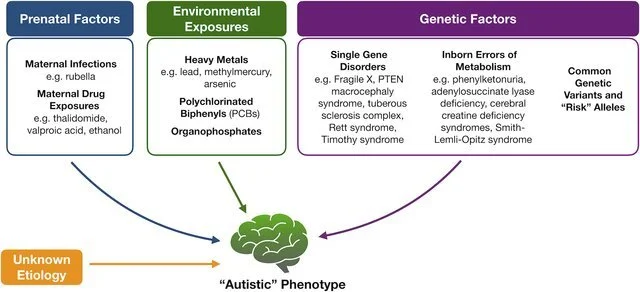
Erros inatos do metabolismo (EIM) são distúrbios genéticos que afetam processos bioquímicos básicos. Estudos mostram que podem estar associados a comportamentos do autismo (TEA).
Embora o TEA tenha causas complexas (genéticas, ambientais, epigenéticas) e, em muitos casos, a etiologia permaneça desconhecida, os autores ressaltam que alguns casos podem ter origem metabólica tratável ou parcialmente tratável (Zigman et al., 2021).
Em muitos EIM, há sintomas do sistema nervoso central (mais de 50% dos pacientes) ou manifestações psiquiátricas. Em alguns casos, pacientes com EIM apresentam sintomas de TEA ou características autísticas.
No entanto, para TEA “não-sindrômico” (sem outros sinais clínicos óbvios além de autismo), a prevalência de EIM é baixa (<0,5%) segundo alguns estudos.
Tipos de EIM associadas ao TEA
Aminoácidos/metabolismo de transportadores: ex. Fenilcetonuria (PKU) — se não tratada, pode levar a deficiência intelectual e traços autísticos.
Distúrbios do ciclo da ureia — hiperamonemia que afeta o cérebro, podendo levar a sintomas neurológicos e comportamentais.
Distúrbios da biossíntese de colesterol — por exemplo Síndrome de Smith‑Lemli‑Opitz (SLOS) que tem frequentemente características de autismo.
Distúrbios mitocondriais e de energia — disfunção mitocondrial aparece com frequência em pacientes com TEA.
Distúrbios de neurotransmissores, purinas, creatina, etc.
Diagnóstico e abordagem terapêutica
Em casos de TEA com características “sindrômicas” (ou seja, com outros sinais clínicos neurológicos ou somáticos), deve haver avaliação de EIM — histórico clínico, exame neurológico, exames metabólicos básicos (aminoácidos plasmáticos, ácidos orgânicos urinários, acilcarnitinas, etc).
As terapias possíveis variam conforme o distúrbio: dieta de restrição (ex: na PKU), suplementação de co-fatores, terapia de reposição enzimática, transplante de órgão em casos selecionados.
Em particular, destacam-se seis princípios terapêuticos gerais: (1) redução do substrato tóxico, (2) remoção de metabólitos tóxicos, (3) suplementação do produto faltante, (4) estímulo da atividade enzimática deficiente, (5) terapia de reposição enzimática, (6) transplante de órgão.
Para famílias e profissionais que lidam com TEA, é importante lembrar que nem todos os casos são “apenas genéticos/ambientais”: há uma fatia que pode ter causas metabólicas tratáveis — o que abre esperança de intervenção precoce.
Valorize a avaliação detalhada: se existir atraso global, regressão, outros sinais neurológicos (convulsões, ataxia), ou sinais somáticos (problemas metabólicos, digestivos, etc), considerar encaminhamento para avaliação metabólica/genética.
Embora algumas crianças com TEA terem erros inatos do metabolismo identificáveis, isso representa apenas uma pequena fração dos casos (estima-se até ~5%). Porém, estudos metabolômicos mais amplos têm relacionado alterações em aminoácidos (glicina, taurina), metabolismo energético (succinato) ao TEA.
Estes estudos mostram evidências de possíveis disfunções mitocondriais, de fosforilação oxidativa e de estresse oxidativo em grupos com TEA. Mostram também alterações associadas ao microbioma intestinal.