A Síndrome dos Ovários Policísticos (SOP) é uma condição multifatorial que afeta milhões de mulheres em idade reprodutiva, caracterizada por desequilíbrios hormonais, resistência à insulina e disfunções ovulatórias. Um estudo trouxe à tona um possível elo até então pouco explorado: a proteína zonulina.
O que é a zonulina?
Zonulina é uma proteína que regula a permeabilidade do intestino. Níveis elevados de zonulina estão associados à hiperpermeabilidade intestinal, também conhecida como "intestino permeável", uma condição que pode desencadear inflamações sistêmicas.
Principais achados do estudo:
Mulheres com SOP apresentaram níveis significativamente mais altos de zonulina no sangue, quando comparadas a mulheres sem a síndrome.
Esses níveis elevados estavam positivamente correlacionados com a resistência à insulina — um dos pilares metabólicos da SOP.
Além disso, quanto maior a concentração de zonulina, mais severas eram as anovulações (ausência de ovulação), sugerindo que a zonulina pode estar ligada à disfunção reprodutiva observada na SOP.
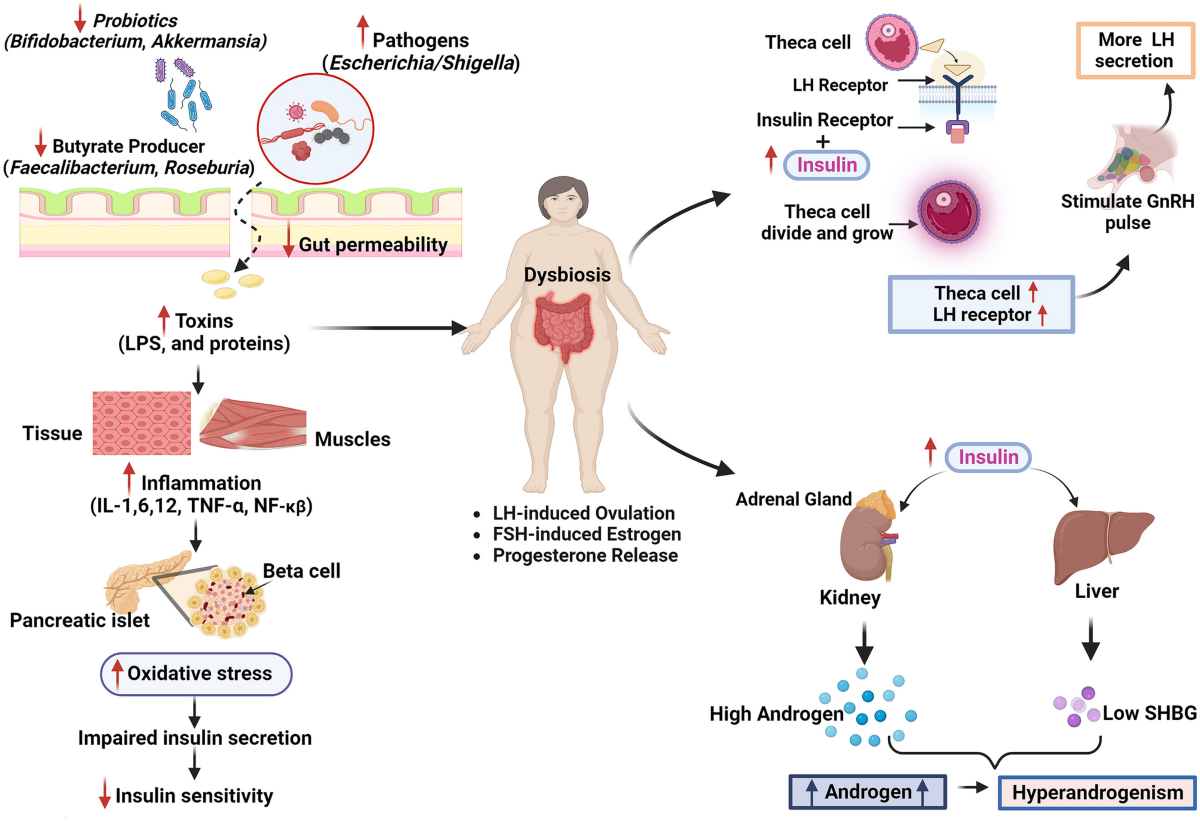
A SOP também leva à disbiose, reduzindo a diversidade microbiana e os micróbios benéficos, como Faecalibacterium, Roseburia, Akkermenisa e Bifidobacterium, e causando uma maior carga de patógenos oportunistas, como Escherichia/Shigella, Fusobacterium, Bilophila e Sutterella.
O intestino associado à SOP apresenta níveis mais elevados da enzima microbiana intestinal β-glucuronidase, causando a desglucuronidação do andrógeno conjugado, tornando-o suscetível à reabsorção pela circulação entero-hepática, levando a um nível mais alto de andrógeno no sistema circulatório.
De modo geral, na SOP, essa disbiose aumenta a permeabilidade intestinal e o LPS na circulação sistêmica, o N-óxido de trimetilamina (TMAO) no sistema circulatório, a inflamação crônica no tecido adiposo e no fígado, e o estresse oxidativo e o acúmulo de lipídios no fígado. Assim, em mulheres com SOP, a disbiose pode promover a progressão e a gravidade do diabetes tipo 2, da doença hepática gordurosa não alcoólica (DHGNA) e das doenças cardiovasculares (DCV).
Para aliviar essas complicações associadas à SOP, terapêuticas microbianas (modulação intestinal com pré e probióticos ou transplante de microbioma fecal) podem ser usadas sem quaisquer efeitos colaterais, ao contrário do que ocorre com a terapia hormonal. A zonulina também poderia ser um novo marcador clínico e, quem sabe, até um alvo terapêutico futuro.